引 言
1 实验部分
1.1 实验材料与仪器
1.1.1 实验材料
1.1.2 实验仪器
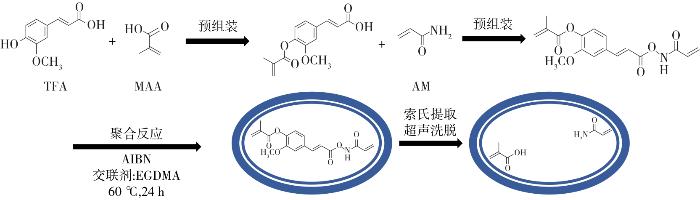
1.2 MIP的制备
1.2.1 模板分子预组装
1.2.2 聚合反应
1.2.3 模板洗脱与后处理
1.3 SGO的制备
1.4 SGO/MIP复合膜的制备
表1 SGO/MIP复合膜的配方Table 1 Formulation of the SGO/MIP composite membranes |
| 复合膜 | MIP 质量/g | SGO 质量/g | PVDF 质量/g | 致孔剂 |
|---|---|---|---|---|
| SGO/MIP1 | 0.225 | 0.9 | 12 | 3% PVP |
| SGO/MIP2 | 0.225 | 0.9 | 12 | 10% PVP |
| SGO/MIP3 | 0.225 | 0.9 | 12 | 4.5% PEG2000 |
| SGO/MIP4 | 0.225 | 0.9 | 12 | 6% PEG2000 |
| 对照组 | 0 | 0.9 | 12 | 3% PVP |
1.5 单功能单体和双功能单体MIP的吸附能力测定
1.5.1 聚合反应
表2 分子印迹聚合物的配方Table 2 Formulation of the molecularly imprinted polymers |
| 聚合物 | n(TFA)/ mmol | n(MAA)/ mmol | n(AM)/ mmol | n(EGDMA)/ mmol | m(AIBN)/ mg |
|---|---|---|---|---|---|
| MIP1 | 1 | 8 | 0 | 20 | 10 |
| MIP2 | 1 | 0 | 5 | 20 | 10 |
| MIP3 | 1 | 8 | 5 | 20 | 10 |
| NIP | 0 | 8 | 5 | 20 | 10 |
1.5.2 模拟液静态吸附实验
1.6 GO、SGO和SGO/MIP复合膜的表征
1.7 膜渗透实验
1.8 发酵液中TFA的分离纯化
1.8.1 动态膜分离
1.8.2 梯度洗脱
1.8.3 重结晶
1.9 TFA纯度测定
表3 流动相梯度Table 3 Mobile phase gradient |
| 时间/min | 体积分数/% | |
|---|---|---|
| 甲醇 | 0.1%甲酸水溶液 | |
| 0 | 15 | 85 |
| 15 | 15 | 85 |
| 20 | 50 | 50 |
| 25 | 100 | 0 |
| 26 | 100 | 0 |
| 30 | 15 | 85 |
| 50 | 15 | 85 |
1.10 TFA的鉴定
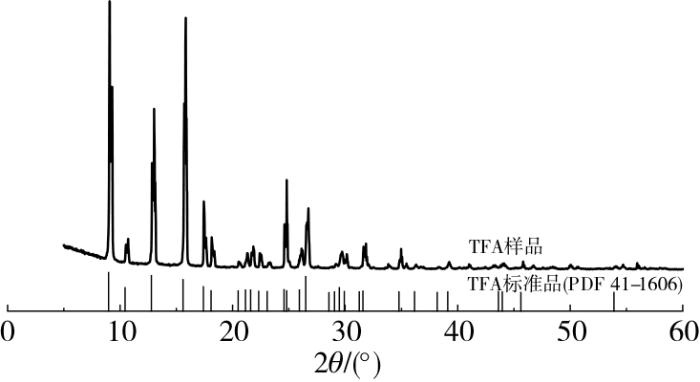
1.10.1 晶体结构
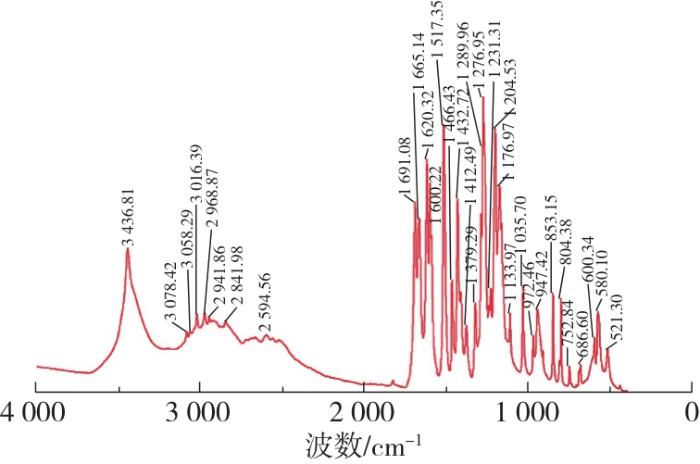
1.10.2 官能团
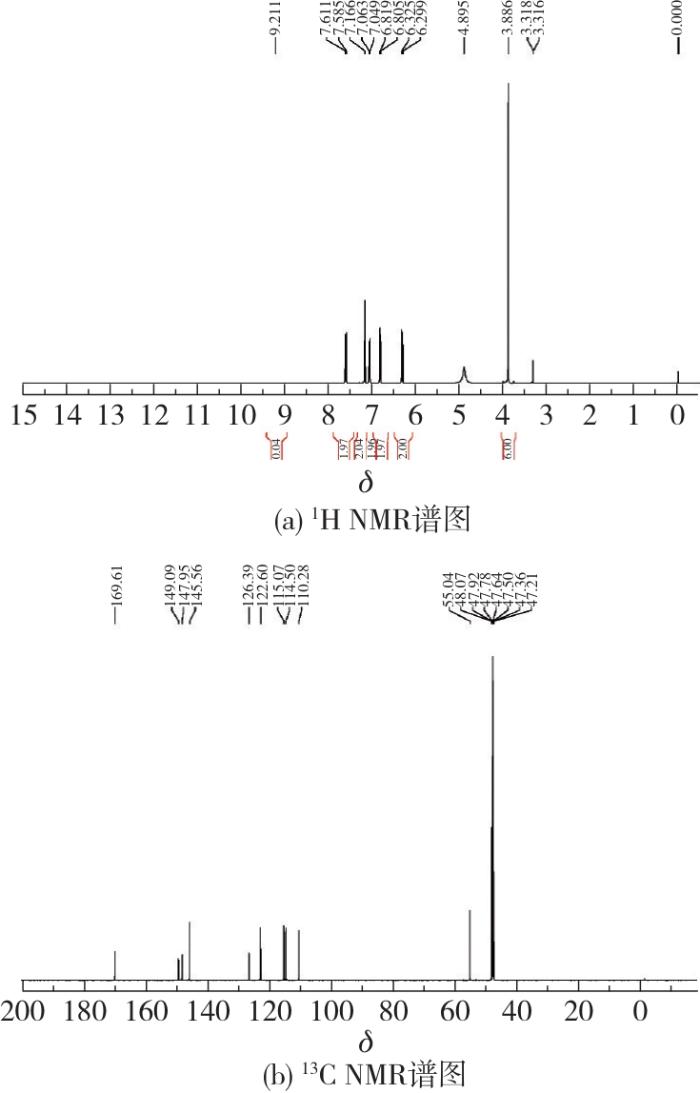
1.10.3 化学结构
2 结果与讨论
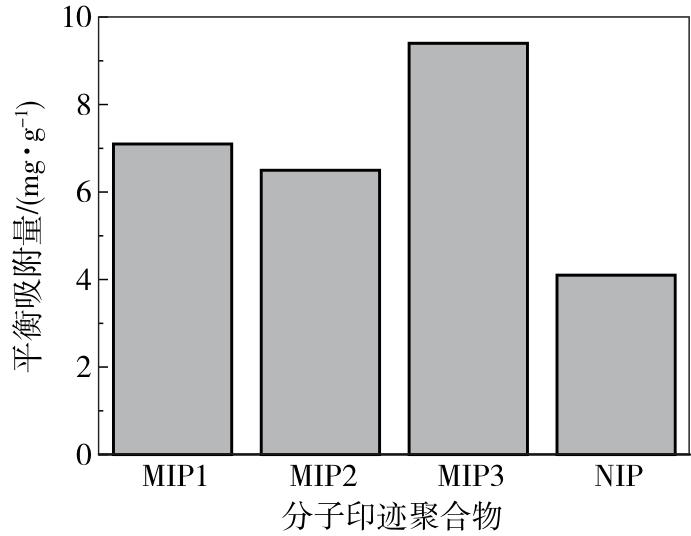
2.1 MIP的静态平衡吸附量
2.2 GO、SGO和SGO/MIP复合膜的表征结果
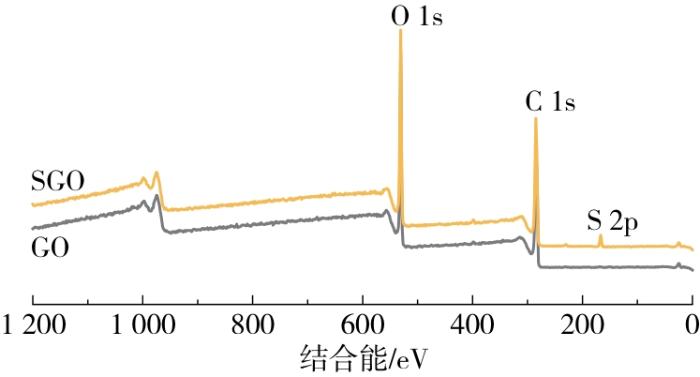
2.2.1 XPS谱图和Zeta电位
2.2.2 水接触角
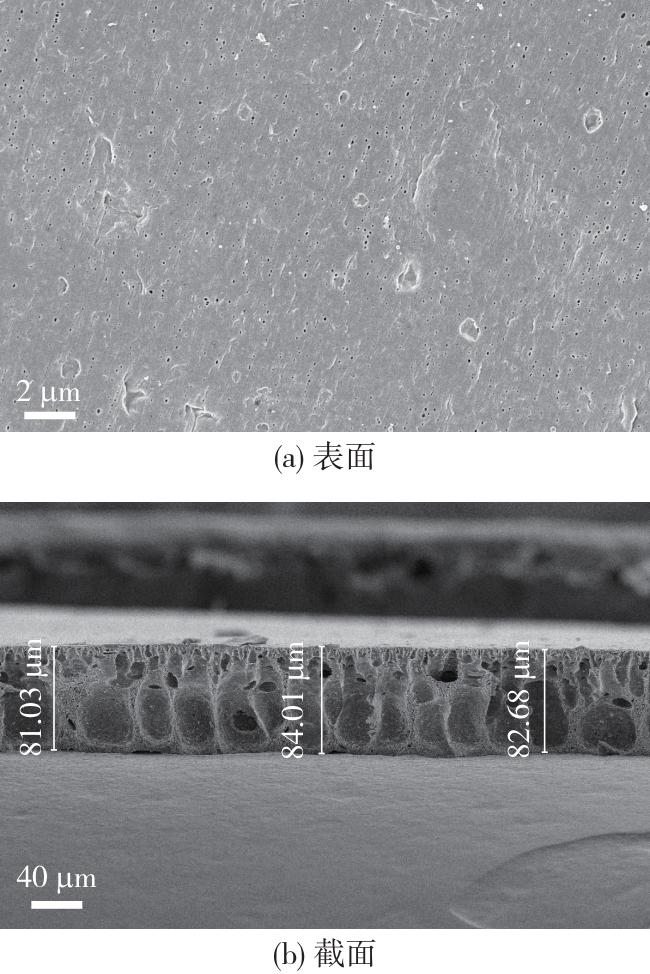
2.2.3 微观形貌和元素分布
2.3 SGO/MIP复合膜的吸附性能
表4 SGO/MIP复合膜的吸附容量和膜通量Table 4 Adsorption capacity and membrane flux of SGO/MIP composite membranes |
| 复合膜 | 吸附容量/(mg·m-²) | 膜通量(25 ℃)/ (L·m-²·h-1) | |
|---|---|---|---|
| 25 ℃ | 37 ℃ | ||
| SGO/MIP1 | 2 002.36 | 1 652.32 | 44.86 |
| SGO/MIP2 | 2 118.78 | 1 800.56 | 64.43 |
| SGO/MIP3 | 2 152.55 | 1 683.18 | 40.57 |
| SGO/MIP4 | 2 249.31 | 1 939.04 | 53.94 |
| 对照组 | 1 204.76 | 806.99 | 42.48 |
2.4 TFA的纯度和回收率
表5 TFA的纯度和回收率Table 5 Purity and recovery of TFA |
| 复合膜 | TFA纯度/% | TFA回收率/% |
|---|---|---|
| SGO/MIP1 | 95.6 | 86.50 |
| SGO/MIP2 | 96.2 | 86.13 |
| SGO/MIP3 | 95.4 | 86.34 |
| SGO/MIP4 | 96.4 | 87.17 |