2. 新疆储能与光电催化材料重点实验室, 乌鲁木齐 830054
2. Xinjiang Key Laboratory of Energy Storage and Photoelectric Catalytic Materials, Urumqi 830054, China
随着工业生产的飞速发展,大量的废水被排放到水环境中。在农业灌溉过程中,重金属离子(例如汞、砷、镉、铅、铜、钴等离子)对水质的污染严重危害农作物生长,影响农产品的产量及质量,从而威胁到人类的身体健康。因此,对水体中的重金属离子进行有效处理引起了人们的高度关注[1-4]。目前,废水中重金属离子污染物的处理方法有化学沉淀法、离子交换法、膜过滤法和电化学法等[5]。其中,电化学法具有处理速度快、无二次污染、可以利用各类重金属的独立氧化还原电位而选择性地回收某些贵重金属等优势,因此广泛应用于工业废水处理领域[6-7],并表现出较好的重金属去除效果[7-13]。
电极活性材料对电化学法去除水中重金属污染物的效果有着重要的影响[14]。目前,文献报道的在电化学法中使用的电极材料主要有原子层沉积TiO2涂层不锈钢网[15]、金属氧化物包覆钛网[16]、金属/金属氧化物复合物[17]、石墨[13]等。导电聚合物是具有共轭π键的一类高分子化合物,具有交替单双(或三)键的连续π-π共轭主链结构特征,因此其电化学性能优异[18]。导电聚合物具有独特的氧化还原特性、良好的导电能力以及使用轻便等优势,因此在电化学法去除水体重金属污染物方面具有潜在的应用价值。目前,导电聚合物主要在化学吸附法中用于去除水溶液中的重金属离子[19-22],但是在电化学法中将导电聚合物用作电极材料的报道很少。
聚邻苯二胺(poly(o-phenylenediamine),PoPD)的分子链含有丰富的自由氨基和毗邻的亚胺基,它们与金属离子能产生很强的螯合作用,同时可将氧化性金属离子还原,实现对重金属离子的去除[23-25]。Li等[25]考察了化学氧化法制得的PoPD微球对Hg(Ⅱ)的吸附行为,结果表明PoPD微球对Hg(Ⅱ)的吸附量达394 mg/g,去除率为96.7%。Wang等[26]研究了PoPD微球对Cr(VI)的去除效果,在pH小于4的条件下仅在1.5 h内PoPD微球对Cr(VI)的去除率便达到99.04%。Han等[27]制备了空心和实心两种PoPD亚微球,它们对Pb(Ⅱ)的吸附量分别达到103.2 mg/g和101.3 mg/g,去除率均高于90%;但是空心PoPD亚微球对Cu(Ⅱ)和Cd(Ⅱ)的去除率均不太高,仅为60%左右。Rahman等[28]制备了PoPD/水合氧化锆复合颗粒,其对Cd(Ⅱ)的饱和吸附量达到66.66 mg/g。本课题组制备了PoPD/碳点复合物(PoPD/CDs),并采用化学吸附法去除水溶液中的Cu(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ),结果表明PoPD/CDs对这3种离子的去除率分别达到88.16%、98.97%和77.48%[29-30]。
为了进一步提高PoPD对水中重金属污染物的去除效果,本文将PoPD进行交联并用于电化学方法去除重金属离子。电化学方法对于所用的电极活性材料有着较高的要求,例如电极材料应具有较大的比表面积和较宽的孔道以便金属离子顺利嵌入/脱除。显然,通过对聚合物进行交联形成网络结构为可取的改进方法之一。另外,材料表面的配位(螯合)位点在聚合物类吸附材料去除重金属离子方面起着主要作用,因此本文选用可提供富氮官能团的氮丙啶作为交联剂,这将有利于提高材料对重金属离子的物理和化学吸附能力,同时结合导电聚合物独特的电化学氧化还原优势,可以满足电化学法对电极活性材料的要求,实现水溶液中重金属离子的高效电沉积去除。基于此,本文设计并制备了具有空间网状结构的交联PoPD,通过增大材料的比表面积和离子扩散通道以及通过交联及交联剂开环增加吸附活性位点,提高其作为电沉积用电极活性材料去除水中重金属离子的性能。
1 实验部分 1.1 实验原料邻苯二胺(oPD),阿法埃莎天津化学有限公司;过硫酸铵(APS),天津市光复科技发展有限公司;对甲苯磺酸(TsOH),上海山浦化工有限公司;三官能团氮丙啶交联剂(C21H35N3O6),上海麦克林生化科技有限公司;98%浓硫酸(H2SO4),天津永晟精细化工有限公司;氢氧化钠(NaOH),东菀市科兴贸易有限公司;铜标准溶液(1 000 μg/mL),国家有色金属及电子材料分析测试中心。试剂均为分析纯,实验用水均为去离子水。
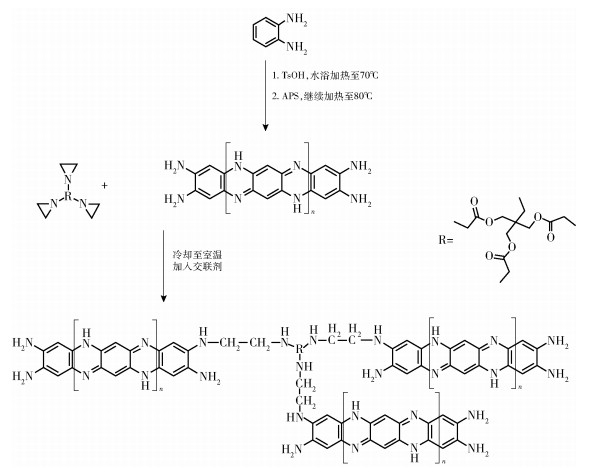
1.2 PoPD及交联PoPD的制备PoPD采用文献[31]的方法制得。交联PoPD采用以下方法制备:取一定质量的oPD单体和TsOH,在圆底烧瓶中用去离子水溶解,水浴加热至70 ℃。然后将一定质量的APS用去离子水溶解(n(APS) ∶n(oPD) ∶n(TsOH)=2 ∶1 ∶1),缓慢滴加到圆底烧瓶中,逐步升温至80 ℃,反应3 h后停止加热并冷却至室温。加入三官能团氮丙啶交联剂(交联剂的质量为oPD单体质量的3%),混合均匀后在培养皿中用红外灯照射12 h,然后真空干燥7 d。交联PoPD的合成路线如图 1所示。
|
图 1 交联PoPD的合成路线 Fig.1 Synthetic route of crosslinked PoPD |
红外吸收光谱(FT-IR) 使用TENSOR-27型红外光谱仪(德国Bruker公司)测定样品的红外吸收光谱,样品用溴化钾(KBr)压片,波数扫描范围为400~4 000 cm-1。
紫外-可见吸收光谱(UV-Vis) 使用UV3600型紫外-可见吸收光谱仪(日本岛津公司)测定样品的紫外-可见吸收光谱,波长扫描范围为200~800 nm。
X-射线粉末衍射(XRD) 使用D8型X-射线粉末衍射仪(德国Bruker公司)测定样品的XRD谱图,扫描范围为10°~60°,靶材为Cu(λ=0.154 18 nm)。
比表面积和孔径 使用Autosorb-IQ-MP型全自动比表面积和孔径分析仪(BET)(美国康塔仪器有限公司)测定样品的比表面积和孔径。
微观形貌 使用LEO-1430VP型低倍扫描电子显微镜(SEM)(德国蔡司公司)以及H-600型低倍透射电子显微镜(TEM)(日本日立公司)观察交联PoPD的微观形貌;使用JSM-7610FPLUS型热场发射扫描电子显微镜(日本电子株式会社)观察电化学还原前后交联PoPD涂覆电极的微观结构,并进行EDS-mapping测试。
pH值 使用PHS-3C型pH计(上海仪电科学仪器股份有限公司)测定电解液的pH值。
电化学测试 使用CHI-660e型电化学工作站(上海辰华仪器公司)测定样品的电化学活性。
1.4 电极制备及预处理先将石墨电极在细砂纸上打磨光滑,然后按照m(活性物质) ∶m(炭黑) ∶m(聚四氟乙烯(PTFE)乳液)=7 ∶1 ∶1依次称量各物质,将其在玻璃片上充分混合并均匀涂抹在打磨好的石墨电极上,室温条件下干燥24 h后备用。
工作电极使用之前,使用CHI-660e型电化学工作站(上海辰华仪器公司)先在单室的三电极电解池中使用循环伏安法(cyclic voltammetry, CV)扫描3圈,电位窗口为-0.3~1.7 V,扫描速率为50 mV/s。工作电极为交联PoPD涂覆的石墨电极,对电极为R115型铂丝电极,参比电极为232型饱和甘汞电极(SCE)。电解液为100 mL的0.1 mol/L H2SO4溶液,将电解液用磁力搅拌器搅拌,转速为200 r/min。通过CV扫描可以达到活化和清洁电极的目的,同时通过记录CV曲线还能确保得到新鲜的电极表面[32],为后续的电化学还原实验提供方便。
1.5 电化学还原去除Cu(Ⅱ)在100 mL的单室三电极电解池中采用恒电位法还原溶液中的Cu(Ⅱ)。电解液由稀释后的50 mg/L铜标准溶液和0.1 mol/L H2SO4溶液组成,使用0.1 mol/L的NaOH或H2SO4溶液调节和控制电解液的pH值。在电化学还原的过程中使用磁力搅拌器搅拌电解液,转速为200 r/min。电化学还原之后,使用美国赛默飞世尔科技公司的iCAP 6000型电感耦合等离子发射光谱仪(ICP)测定电解液中Cu(Ⅱ)的质量浓度,按照式(1)计算Cu(Ⅱ)的去除率R。所有实验均在室温下进行。
| $ R=\frac{C_0-C_t}{C_0} \times 100 \% $ | (1) |
式中:C0为Cu(Ⅱ)的初始质量浓度,mg/L;Ct为经电化学还原t时间后Cu(Ⅱ)的质量浓度,mg/L。
1.6 交联PoPD涂覆电极的再生性实验将交联PoPD涂覆的石墨电极作为工作电极,在最佳条件下对Cu(Ⅱ)进行电还原10 h。取电还原后的溶液,使用ICP测定溶液中Cu(Ⅱ)的质量浓度(C1),然后将电极电位调整为1 V氧化40 min,可以观察到沉积在电极表面的金属铜逐渐消失,取氧化后的溶液使用ICP测定溶液中Cu(Ⅱ)的质量浓度(C2)。对于每次吸脱附过程,按照式(2)计算脱附率(D)。
| $ D=\frac{C_2-C_1}{C_0-C_1} \times 100 \% $ | (2) |
式中C0为15 mg/L。用去离子水反复冲洗电极,之后在常温下干燥24 h,重复上述操作5次。每次重复使用前,对交联PoPD涂覆的石墨电极在10 mV/s的扫描速率下测试CV曲线以考察其稳定性和电化学行为重现性。
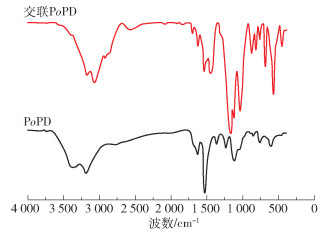
2 结果与讨论 2.1 交联PoPD的表征结果 2.1.1 红外吸收光谱图 2为PoPD和交联PoPD的FT-IR谱图。在PoPD的红外谱图中,3 187 cm-1和3 351 cm-1处的吸收峰为PoPD链上亚氨基和氨基中的N—H伸缩振动峰,在1 626 cm-1处的吸收峰为吩嗪环中C=N的振动吸收峰,在1 521 cm-1处出现了苯环上C=C伸缩振动吸收峰;在1 368 cm-1和1 228 cm-1处的吸收峰是醌环和苯环上的C—N伸缩振动峰,1 122 cm-1处的吸收峰为C—H弯曲振动峰,758 cm-1和606 cm-1处的吸收峰为C—H的面外弯曲振动吸收峰。上述各峰峰值与文献[33-34]基本吻合,表明PoPD制备成功,同时也说明PoPD为类吩嗪结构。从交联PoPD的红外谱图中可以很明显地看到,在3 500~3 100 cm-1处N—H的伸缩振动峰强度增强,这是由于氮丙啶交联剂的加入使得N—H的数量增多所导致;在2 917 cm-1处出现了氮丙啶交联剂链上亚甲基的C—H伸缩振动峰,在1 708 cm-1和1 626 cm-1处的吸收峰是C=O的伸缩振动峰,在1 533 cm-1左右处的吸收峰为N—H的弯曲振动峰[35],在1 438 cm-1处的吸收峰是C—O伸缩振动吸收峰,在1 157 cm-1左右处的吸收峰是C—O—C的不对称伸缩振动吸收峰[2]。上述各峰的存在表明成功制备了交联PoPD。
|
图 2 PoPD和交联PoPD的FT-IR谱图 Fig.2 FT-IR spectra of PoPD and crosslinked PoPD |
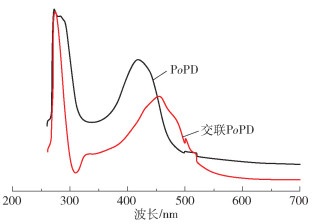
图 3为PoPD和交联PoPD的紫外-可见吸收光谱。在PoPD的UV-Vis光谱中,270 nm处的吸收峰为苯环的E吸收带吸收峰,290 nm处的吸收峰为苯环的B吸收带吸收峰[36];在423 nm处的吸收峰是由类吩嗪结构中氨基官能团上孤对电子的π-π作用引起的[34],这一结果与FT-IR谱图中表明的PoPD为类吩嗪结构相符合。从交联PoPD的UV-Vis光谱中可以看出,交联对270 nm处苯环的E吸收带吸收峰几乎没有产生影响,而苯环的B吸收带吸收峰红移至330 nm处,这可能是交联后聚合物链上的助色基团—NH2增多所致[36];还可以看到交联后类吩嗪结构中氨基官能团上孤对电子的π-π作用使吸收峰红移至455 nm处,这可能是交联剂的加入使得共轭官能团增加所致。
|
图 3 PoPD和交联PoPD的紫外-可见吸收光谱 Fig.3 UV-Vis absorption spectra of PoPD and crosslinked PoPD |
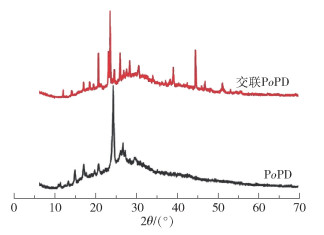
图 4为PoPD和交联PoPD的XRD谱图。从PoPD的谱图中可知,在2θ≈11.04°、13.12°、14.99°、17.06°、20.61°、24.54°、26.63°处出现较为尖锐的衍射峰,其中在2θ≈24.54°处的衍射峰最强,出现的各峰与文献[31]基本一致;PoPD的XRD谱图存在较为对称且尖锐的特征衍射峰,说明PoPD具有较好的结晶性。从交联PoPD的谱图中可以看到,除了具有PoPD的特征衍射峰之外,交联PoPD还出现了一些新的衍射峰;与PoPD相比,交联PoPD的XRD谱图中尖锐的特征峰增多,这是在交联作用下分子链排列更加整齐规律的结果[37]。
|
图 4 PoPD和交联PoPD的XRD谱图 Fig.4 XRD patterns of PoPD and crosslinked PoPD |
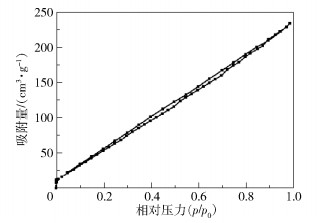
图 5为交联PoPD的N2吸脱附曲线。从图中可以看到,在相对压力较低的区域(p/p0 < 0.1),吸附等温曲线急剧上升,表明材料含有微孔;在中等压力区域(0.1 < p/p0 < 0.9),等温曲线呈现出较为明显的线性增加趋势,同时观察到吸附回滞环,说明材料中有介孔存在。表 1列出了交联PoPD的比表面积、总孔体积和孔径。在本课题组前期的研究中测得PoPD的比表面积为119.89 m2/g[30],而本实验测得交联PoPD的比表面积为308.33 m2/g,显著大于PoPD,这可能是因为颗粒之间发生交联后形成了更多的介孔。
|
图 5 交联PoPD的N2吸脱附曲线 Fig.5 N2 adsorption-desorption curves of crosslinked PoPD |
| 下载CSV 表 1 交联PoPD的比表面积、总孔体积和平均孔径 Table 1 Specific surface area, total pore volume and average pore size of crosslinked PoPD |
图 6(a)和6(b)分别为交联PoPD的SEM图和TEM图。由图 6(a)可以看到,交联PoPD呈现出重瓣花型结构,并且表面粗糙,具有较多凹凸不平的褶皱,同时还含有很多堆积孔。由图 6(b)可以看到,交联PoPD呈现棒状结构并且堆积严重。

|
图 6 交联PoPD的SEM图和TEM图 Fig.6 SEM and TEM images of crosslinked PoPD |
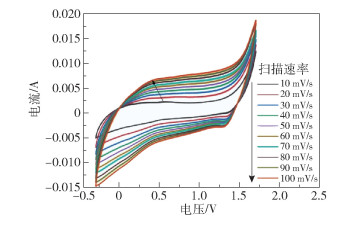
图 7为交联PoPD在不同扫描速率下的循环伏安曲线。从图中可以观察到明显的氧化还原峰,表明交联PoPD具有一定的法拉第准电容行为;在电位窗口为-0.3~1.7 V、扫描速率为10~100 mV/s的范围内,CV曲线的面积随着扫描速率的增大而增大,阴阳极的峰电流也随着扫描速率的增大而增大,表明电容发生一定程度的衰减,这可能是由于在充放电的循环过程中,频繁的溶胀收缩破坏了聚合物的离子迁移通道,导致结构坍塌[38]。
|
图 7 交联PoPD在不同扫描速率下的循环伏安曲线 Fig.7 Cyclic voltammetry curves of crosslinked PoPD at different scanning rates |
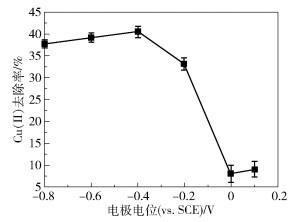
图 8为不同的电极电位对交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)效果的影响。由结果可知,交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)的最佳电极电位为-0.4 V。当电极电位在-0.8~-0.4 V之间时,交联PoPD电化学还原去除Cu(Ⅱ)的效率呈现出缓慢增加的趋势;当电极电位大于-0.4 V时,交联PoPD对Cu(Ⅱ)的去除率急剧下降;当电极电位大于0 V时,Cu(Ⅱ)的去除率非常低。这可能是因为当电极电位不断增大时,交联PoPD在电化学还原的过程中发生了部分不可逆的降解,进而降低了交联PoPD对Cu(Ⅱ)的电化学还原能力[39],导致去除率下降。
|
图 8 电极电位对Cu(Ⅱ)去除率的影响 Fig.8 Effect of electrode potential on Cu(Ⅱ) removal rate |
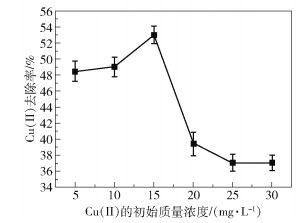
图 9为电解液中Cu(Ⅱ)的初始质量浓度对交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)效果的影响。可以看出,交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)的最佳初始质量浓度为15 mg/L。随着Cu(Ⅱ)初始质量浓度的增加,去除率呈现出先增大后减小的趋势。这可能是由于当Cu(Ⅱ)的初始质量浓度小于15 mg/L时,随着电解液浓度的增大,离子数目增多,电导率不断增大,因此去除率增大。当电解液中Cu(Ⅱ)的初始质量浓度较低时,铜的传质速率较为缓慢,同时由式(3)[40]可知,较低的Cu(Ⅱ)初始质量浓度导致铜的实际还原电位较低,使铜的沉积效率低下,因此去除率没有达到最佳。但是当电解液中Cu(Ⅱ)的初始质量浓度大于15 mg/L时去除率反而降低,这可能是因为除了交联PoPD对Cu(Ⅱ)的吸附外,电化学反应进程也会影响Cu(Ⅱ)的去除效果:阳极上水参与电极反应而产生氧气与氢离子,不可避免地腐蚀沉积在阴极表面上的金属铜,使得铜以Cu(Ⅱ)的形式进入溶液,脱离交联PoPD电极表面,因此去除率降低。
| $ E=E^0+\frac{R T}{n F} \ln \frac{c}{c^\mathtt{θ}}-\eta_{\mathrm{K}} $ | (3) |
|
图 9 Cu(Ⅱ)的初始质量浓度对Cu(Ⅱ)去除率的影响 Fig.9 Effect of initial mass concentration of Cu(Ⅱ) on Cu(Ⅱ) removal rate |
式中:E为阳离子放电的实际电位, V;E0为标准电极电位, V;R为摩尔气体常数,8.314 J/(mol·K);T为温度, K;n为电化学反应中电子的计量系数;F为法拉第常数,9.648×104 C/mol;c为阳离子在溶液中的浓度, mol/L;cθ为标准浓度,1mol/L;ηK为阳离子在阴极的过电位,V。
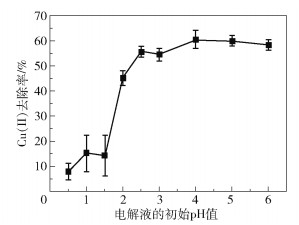
2.2.3 电解液的初始pH值图 10为电解液的初始pH值对交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)效果的影响。可以看出,交联PoPD涂覆的石墨电极电化学还原Cu(Ⅱ)的最佳pH值为4;当pH值在0.5~4之间时,交联PoPD对Cu(Ⅱ)的去除率呈上升趋势;当pH值大于4时,交联PoPD对Cu(Ⅱ)的去除率呈缓慢下降的趋势。这是因为当电解液的pH值越低时,溶液中的H+浓度越高,而在水溶液中H+的迁移速度比其他离子快得多,在电场力的作用下,大量的H+和H3O+占据了吸附剂表面具有吸附作用的活性位点,阻碍了Cu(Ⅱ)到达阴极表面,从而降低了Cu(Ⅱ)的去除率[41];随着pH值的升高,电解液中H+浓度降低,阴极表面的阳离子总量减少,此时Cu(Ⅱ)会比较容易地到达阴极表面而析出,因此当电解液的pH值适当增大时,Cu(Ⅱ)的去除率增大。但是当电解液的pH值过高时,Cu(Ⅱ)可能会发生水解,甚至在电极附近生成蓝色沉淀,进而影响Cu(Ⅱ)的还原,所以电解液的pH值过低或过高都不利于Cu(Ⅱ)的还原[42-43]。因此,在电化学还原的过程中应选择合适的电解液pH值以确保较高的Cu(Ⅱ)去除率。
|
图 10 电解液的初始pH值对Cu(Ⅱ)去除率的影响 Fig.10 Effect of initial pH value of the electrolyte on Cu(Ⅱ) removal rate |
图 11为电化学还原Cu(Ⅱ)后残液的pH值分布。可以看出,当溶液的初始pH值在0.5~3之间时,电还原结束后溶液的pH值大于溶液的初始pH值,这可能是因为此时电解液中的H+浓度相对较高,使析氢反应加剧,因此电解液的pH值会稍微增加。当溶液的初始pH值在4~6之间时,电化学还原后电解液的pH值小于电解液的初始pH值,这是因为随着溶液的pH值增大,溶液中的H+浓度降低,此时析氢反应不容易发生,同时在电化学还原的过程中也会在阳极生成大量的H+,因此溶液的pH值减小。

|
图 11 电化学还原后残液的pH值分布 Fig.11 pH value distribution of the residual electrolyte after electrochemical reduction |
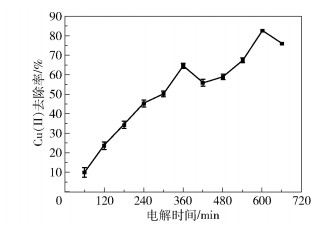
图 12给出了电解时间对交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)效果的影响。可以看出,交联PoPD涂覆的石墨电极电化学还原去除Cu(Ⅱ)的最佳电解时间为10 h,去除率为83.28%。随着电解时间的增加,Cu(Ⅱ)的去除率呈现出先增加后减小的趋势。这可能是因为电化学还原刚开始进行时,溶液中的Cu(Ⅱ)浓度相对较高,铜的实际还原电位也相对较高,因此去除率呈增加趋势。但是随着溶液中Cu(Ⅱ)的不断析出,Cu(Ⅱ)浓度逐渐降低,电极极化或浓差极化严重,导致析铜的过电位不断升高,电化学还原铜的反应速率随之减小。同时,在电还原的过程中也会在阳极生成一定的H+,在电场的作用下H+不断地向阴极聚集,与Cu(Ⅱ)争夺电子,从而发生析氢竞争反应。
|
图 12 电解时间对Cu(Ⅱ)去除率的影响 Fig.12 Effect of electrolysis time on Cu(Ⅱ) removal rate |
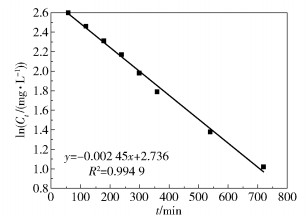
根据准一级动力学模型(式(4))[32]对交联PoPD电化学还原去除Cu(Ⅱ)的过程进行拟合,拟合曲线如图 13所示。决定系数R2=0.994 9,表明交联PoPD电化学还原去除Cu(Ⅱ)的过程符合准一级动力学。k1=2.45×10-3 min-1,说明Cu(Ⅱ)的电化学还原速率较为缓慢,这可能是因为Cu(Ⅱ)的电化学还原是在电极表面上发生电子转移的过程,而暴露于电解液中的电活性物质的面积比较小[32]。
| $ r=k_1 C_t $ | (4) |
|
图 13 准一级动力学拟合曲线 Fig.13 Quasi-first-order kinetic simulation curve |
式中:r为电化学还原去除Cu(Ⅱ)的速率,mg/(L ·min);k1为准一级动力学速率常数,min-1。
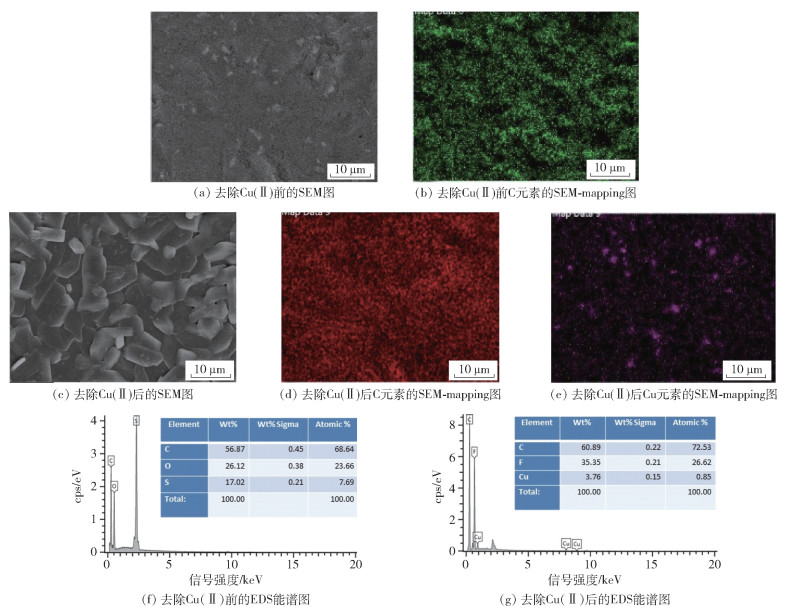
2.3 电化学还原去除Cu(Ⅱ)前后交联PoPD涂覆电极的结构表征结果图 14为交联PoPD涂覆的石墨电极在电化学还原去除Cu(Ⅱ)前后的SEM图、SEM-mapping图和EDS能谱图。从图 14(a)中可以看出,在电化学还原Cu(Ⅱ)之前,交联PoPD涂覆的石墨电极表面并没有观察到明显的沉积物。图 14(c)中,在电化学还原Cu(Ⅱ)之后,石墨电极表面出现棒状结构的沉积物,形状较为规则,这可能是因为电极电位较小,铜在电极上沉积的速度较为缓慢,因此铜在电极表面呈晶体状均匀析出。从SEM-mapping图(图 14(b)、14(d)、14(e))和EDS能谱图(图 14(f)、14(g))中可以看到,在电化学还原Cu(Ⅱ)前后交联PoPD涂覆的电极都含有碳元素,电化学还原后电解液中的Cu(Ⅱ)被交联PoPD所吸附,并且电化学还原为Cu而析出,较为均匀地附着在电极上。
|
图 14 交联PoPD涂覆石墨电极去除Cu(Ⅱ)前后的SEM图、SEM-mapping图和EDS能谱图 Fig.14 SEM images, SEM-mapping images and EDS spectra of the PoPD-coated graphite electrode before and after Cu(Ⅱ) removal |
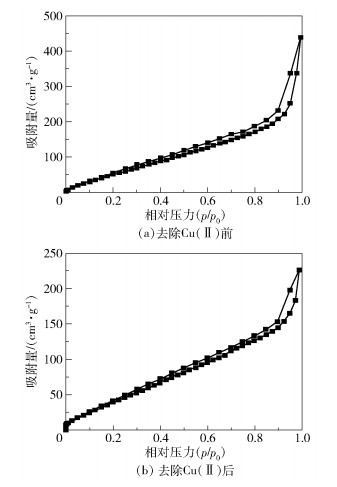
图 15(a)和15(b)分别为交联PoPD涂覆的石墨电极在电化学还原去除Cu(Ⅱ)前后的N2吸脱附曲线。从图中可以看到,交联PoPD涂覆的石墨电极在电化学还原Cu(Ⅱ)前后具有类似的吸脱附曲线,说明电化学还原之后并没有改变材料的孔结构。在低压区域(p/p0 < 0.1),交联PoPD电化学还原Cu(Ⅱ)前后的吸附等温曲线均表现为急剧上升的趋势,表明电化学还原前后的材料都含有微孔结构;在中压区(0.1 < p/p0 < 0.9),吸附等温曲线呈现出线性增加的趋势,并且均出现了吸附回滞环,说明材料有介孔存在[38]。表 2为交联PoPD在电化学还原前后的比表面积、总孔体积和平均孔径。由表 2可知,交联PoPD在电化学还原去除Cu(Ⅱ)前具有巨大的比表面积,这将有利于增强物理吸附[44]。电化学还原去除重金属离子的整个过程包括电解质溶液内的扩散过程、电极表面的物理吸附过程和电化学反应过程,因此物理吸附过程的增强必定有利于提高Cu(Ⅱ)的去除效率。在去除Cu(Ⅱ)后交联PoPD的比表面积、总孔体积和平均孔径均明显增大,这可能是由于在电化学还原的过程中析出的铜附着在电极表面所致。
|
图 15 交联PoPD涂覆的石墨电极去除Cu(Ⅱ)前后的N2吸脱附曲线 Fig.15 N2 adsorption-desorption curves of crosslinked PoPD-coated graphite electrode before and after Cu(Ⅱ) removal |
| 下载CSV 表 2 交联PoPD在去除Cu(Ⅱ)前后的比表面积、总孔体积和平均孔径 Table 2 Specific surface area, total pore volume and average pore size of crosslinked PoPD before and after Cu(Ⅱ) removal |
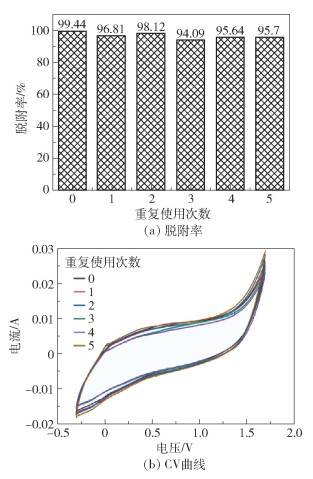
图 16(a)为交联PoPD作为电极材料在最佳条件下重复使用5次的脱附率,可以看出交联PoPD在重复使用5次后脱附率大于94.09%,呈现较高的回收再生性能。图 16(b)为交联PoPD涂覆的石墨电极重复使用5次的循环伏安曲线,可以观察到石墨电极在重复使用5次后氧化还原峰没有明显变化并且重合度较高,表明交联PoPD涂覆的石墨电极具有良好的稳定性以及电化学行为重现性。
|
图 16 交联PoPD涂覆的石墨电极的回收及再生性能 Fig.16 Recovery and regeneration performance of crosslinked PoPD-coated graphite electrode |
(1) 经交联改性成功制得导电聚合物基吸附材料——交联PoPD。与PoPD相比,交联PoPD具有独特的电化学氧化还原特性以及高比表面积的介孔结构。
(2) 采用三电极体系,以交联PoPD涂覆的石墨电极为工作电极,利用恒电位法经电化学还原电沉积去除Cu(Ⅱ)。筛选出电化学还原的最适宜条件,在此条件下Cu(Ⅱ)去除率可达83.28%,并且电沉积过程遵循准一级动力学模型。
(3) 所得交联PoPD的制备过程简便,再生性能良好,经5次重复使用后脱附效率仍保持在94.09%以上,在水体重金属离子的电化学法去除方面具有一定的应用潜能。
| [1] |
LIU C, WU T, HSU P C, et al. Direct/alternating current electrochemical method for removing and recovering heavy metal from water using graphene oxide electrode[J]. ACS Nano, 2019, 13(6): 6431-6437. DOI:10.1021/acsnano.8b09301 |
| [2] |
KAKORIA A, SINHA-RAY S, SINHA-RAY S. Industrially scalable chitosan/nylon-6 (CS/N) nanofiber-based reusable adsorbent for efficient removal of heavy metal from water[J]. Polymer, 2021, 213(1-2): 123333. |
| [3] |
廖晓峰, 钟静萍, 陈云嫩, 等. 功能化凹凸棒吸附材料的制备及其对重金属废水中Pb2+的吸附行为[J]. 环境科学, 2022, 43(1): 387-397. LIAO X F, ZHONG J P, CHEN Y N, et al. Preparation of functional attapulgite composite and its adsorption behaviors for Congo red[J]. Environmental Science, 2022, 43(1): 387-397. (in Chinese) |
| [4] |
蔡长卿, 金昌盛, 陈佳, 等. 东洞庭湖沉积物重金属污染及生态-健康风险[J]. 农业环境科学学报, 2022, 41(6): 1337-1347. CAI C Q, JIN C S, CHEN J, et al. Sediment heavy metal pollution and its ecological and health risk assessment in the East Dongting Lake, China[J]. Journal of Agro-Environment Science, 2022, 41(6): 1337-1347. (in Chinese) |
| [5] |
HUANG S Y, FAN C S, HOU C H. Electro-enhanced removal of copper ions from aqueous solutions by capacitive deionization[J]. Journal of Hazardous Materials, 2014, 278: 8-15. DOI:10.1016/j.jhazmat.2014.05.074 |
| [6] |
LEE N, LIU M L, WU M C, et al. The effect of the redox potential on the removal characteristic of divalent cations during activated carbon-based capacitive deionization[J]. Chemosphere, 2021, 274: 129762. DOI:10.1016/j.chemosphere.2021.129762 |
| [7] |
DEVI P, DAS U, DALAY A K. In-situ chemical oxidation: principle and applications of peroxide and persulfate treatments in wastewater systems[J]. Science of the Total Environment, 2016, 571: 643-657. DOI:10.1016/j.scitotenv.2016.07.032 |
| [8] |
SU J L, LIN X, ZHENG S L, et al. Mass transport-enhanced electrodeposition for the efficient recovery of copper and selenium from sulfuric acid solution[J]. Separation and Purification Technology, 2017, 182: 160-165. DOI:10.1016/j.seppur.2017.03.056 |
| [9] |
VERDUZCO L E, OLIVA J, OLIVA A I, et al. Enhanced removal of arsenic and chromium contaminants from drinking water by electrodeposition technique using graphene composites[J]. Materials Chemistry and Physics, 2019, 229: 197-209. DOI:10.1016/j.matchemphys.2019.03.006 |
| [10] |
LIU Y X, WU X Y, YUAN D X, et al. Removal of nickel from aqueous solution using cathodic deposition of nickel hydroxide at a modified electrode[J]. Journal of Chemical Technology and Biotechnology, 2013, 88(12): 2193-2200. DOI:10.1002/jctb.4085 |
| [11] |
BHATLURI K K, MANNA M S, GHOSHAL A K, et al. Separation of cadmium and lead from wastewater using supported liquid membrane integrated with in-situ electrodeposition[J]. Electrochimica Acta, 2017, 229: 1-7. DOI:10.1016/j.electacta.2017.01.090 |
| [12] |
LI X H, LI H Y, XU X J, et al. Preparation of a reduced graphene oxide @ stainless steel net electrode and its application of electrochemical removal Pb(Ⅱ)[J]. Journal of the Electrochemical Society, 2017, 164(4): E71-E77. DOI:10.1149/2.1211704jes |
| [13] |
李想, 吴雅琴, 朱圆圆, 等. 电沉积处理含铜强酸废水阴极回收纳米铜[J]. 水处理技术, 2018, 44(3): 34-38. LI X, WU Y Q, ZHU Y Y, et al. Nano-copper recovery at cathode in high acid wastewater containing copper by electro-deposition method[J]. Technology of Water Treatment, 2018, 44(3): 34-38. (in Chinese) DOI:10.16796/j.cnki.1000-3770.2018.03.008 |
| [14] |
于栋, 罗庆, 苏伟, 等. 重金属废水电沉积处理技术研究及应用进展[J]. 化工进展, 2020, 39(5): 1938-1949. YU D, LUO Q, SU W, et al. A review on research and application of electrodeposition for heavy metal wastewater treatment[J]. Chemical Industry and Engineering Progress, 2020, 39(5): 1938-1949. (in Chinese) DOI:10.16085/j.issn.1000-6613.2019-1332 |
| [15] |
FAN T Z, DENG W, FENG X H, et al. An integrated electrocoagulation—Electrocatalysis water treatment process using stainless steel cathodes coated with ultrathin TiO2 nanofilms[J]. Chemosphere, 2020, 254: 126776. DOI:10.1016/j.chemosphere.2020.126776 |
| [16] |
ABOU-SHADY A, PENG C S, BI J J, et al. Recovery of Pb(Ⅱ) and removal of NO3- from aqueous solutions using integrated electrodialysis, electrolysis, and adsorption process[J]. Desalination, 2012, 286: 304-315. DOI:10.1016/j.desal.2011.11.041 |
| [17] |
ZHAO X, GUO L B, HU C Z, et al. Simultaneous destruction of nickel(Ⅱ)-EDTA with TiO2/Ti film anode and electrodeposition of nickel ions on the cathode[J]. Applied Catalysis B: Environmental, 2014, 144: 478-485. DOI:10.1016/j.apcatb.2013.07.038 |
| [18] |
GUO X G, FACCHETTI A. The journey of conducting polymers from discovery to application[J]. Nature Materials, 2020, 19: 922-928. DOI:10.1038/s41563-020-0778-5 |
| [19] |
WANG J, DENG B L, CHEN H, et al. Removal of aqueous Hg(Ⅱ) by polyaniline: sorption characteristics and mechanisms[J]. Environmental Science and Technology, 2009, 43: 5223-5228. DOI:10.1021/es803710k |
| [20] |
BARUAH P, MAHANTA D. Adsorption and reduction: combined effect of polyaniline emeraldine salt for removal of Cr(Ⅵ) from aqueous medium[J]. Bulletin of Materterials Science, 2016, 39(3): 875-882. DOI:10.1007/s12034-016-1204-0 |
| [21] |
LV Q F, HUANG M R, LI X G. Synthesis and heavy-metal-ion sorption of pure sulfophenylenediamine copolymer nanoparticles with intrinsic conductivity and stability[J]. Chemistry—A European Journal, 2007, 13(21): 6009-6018. DOI:10.1002/chem.200700233 |
| [22] |
ZARE E N, LAKOURAJ M M, RAMEZANI A. Efficient sorption of Pb(Ⅱ) from aqueous solution using poly (aniline-co-3-aminobenzoic acid)-based magnetic core-shell nanocomposite[J]. New Journal of Chemistry, 2016, 40: 2521-2529. DOI:10.1039/C5NJ02880A |
| [23] |
MOMINA, AHMAD K. Study of different polymer nanocomposites and their pollutant removal efficiency: review[J]. Polymer, 2021, 217: 123453. DOI:10.1016/j.polymer.2021.123453 |
| [24] |
ZARE E N, MOTAHARI A, SILLANPÄÄ M. Nanoadsorbents based on conducting polymer nanocomposites with main focus on polyaniline and its derivatives for removal of heavy metal ion/dyes: a review[J]. Environmental Research, 2018, 162: 173-195. DOI:10.1016/j.envres.2017.12.025 |
| [25] |
LI X G, MA X L, SUN J, et al. Powerful reactive sorption of silver(Ⅰ) and mercury(Ⅱ) onto poly(o-phenylenediamine) microparticles[J]. Langmuir, 2009, 25: 1675-1684. DOI:10.1021/la802410p |
| [26] |
WANG Z F, LIAO F. Synthesis of poly(ortho-phenylenediamine) fluffy microspheres and application for the removal of Cr(Ⅵ)[J]. Journal of Nanomaterials, 2012, 2012: 682802. |
| [27] |
HAN J, DAI J, GUO R. Highly efficient adsorbents of poly(o-phenylenediamine) solid and hollow sub-microspheres towards lead ions: a comparative study[J]. Journal of Colloid and Interface Science, 2011, 356: 749-756. DOI:10.1016/j.jcis.2011.01.038 |
| [28] |
RAHMAN N, NASIR M. Application of Box-Behnken design and desirability function in the optimization of Cd(Ⅱ) removal from aqueous solution using poly(o-phenylenediamine)/hydrous zirconium oxide composite: equilibrium modeling, kinetic and thermodynamic studies[J]. Environmental Science and Pollution Research, 2018, 25: 26114-26134. DOI:10.1007/s11356-018-2566-1 |
| [29] |
MENG Y, XIAO L, MUSLIM A, et al. Improving the adsorption of poly(o-phenylenediamine) to heavy metal ions in aqueous solution through its composite with carbon dots[J]. Journal of Polymer Research, 2021, 28: 404. DOI:10.1007/s10965-021-02739-z |
| [30] |
MENG Y, ZHONG Q, MUSLIM A. Performance of poly-o-phenylenediamine and its carbon dot composite electrode in the removal of Cu2+ from its aqueous solution[J]. Functional Materials Letters, 2021, 14(6): 2151037. DOI:10.1142/S1793604721510371 |
| [31] |
阿孜古丽·木尔赛力木, 如仙古丽·加马力, 吐尔逊·阿不都热依木, 等. 界面聚合法合成聚邻苯二胺及其表征[J]. 化学研究与应用, 2007, 19(4): 409-412. MUSLIM A, JAMAL R, ABDIRYIM T, et al. Facial synthesis and characterization of poly(o-phenylenediamine)[J]. Chemical Reasearch and Application, 2007, 19(4): 409-412. (in Chinese) DOI:10.3969/j.issn.1004-1656.2007.04.015 |
| [32] |
FANG X H, ZHANG G Q, CHEN J, et al. Electrochemical reduction of hexavalent chromium on two-step electrosynthesized one-dimensional polyaniline nanowire[J]. International Journal of Electrochemical Science, 2012, 7: 11847-11858. |
| [33] |
AZARPOUR H, MOGHADAM P N, EHSANIMEHR S, et al. Novel electrically conductive nanocomposites based on polyaniline and poly(aniline-co-melamine) copolymers grafted on melamine-formaldehyde resin[J]. Iranian Polymer Journal, 2022, 31: 1033-1045. DOI:10.1007/s13726-022-01055-7 |
| [34] |
JIANG K P, MA S H, BI H M, et al. Morphology controllable fabrication of poly-o-phenylenediamine microstructures tuned by the ionic strength and their applications in pH sensors[J]. Journal of Material Chemistry A, 2014, 2: 19208-19213. DOI:10.1039/C4TA04269G |
| [35] |
LIU J, CHEN T W, YANG Y L, et al. Removal of heavy metal ions and anionic dyes from aqueous solutions using amide-functionalized cellulose-based adsorbents[J]. Carbohydrate Polymers, 2020, 230: 115619. DOI:10.1016/j.carbpol.2019.115619 |
| [36] |
邱玉倩, 刘千惠, 韩浩杰, 等. 三嗪超交联聚苯乙烯基多孔聚合物的设计与制备[J]. 功能高分子学报, 2020, 33(6): 554-562. QIU Y Q, LIU Q H, HAN H J, et al. Design and preparation of polystyrene-based porous polymers with triazine crosslinker[J]. Journal of Functional Polymers, 2020, 33(6): 554-562. (in Chinese) |
| [37] |
佟楠楠, 范雪荣, 高卫东, 等. 高能电子束辐射交联丁腈橡胶/聚氯乙烯胶辊生胶[J]. 辐射研究与辐射工艺学报, 2021, 39(1): 010203. TONG N N, FAN X R, GAO W D, et al. High energy electron beam irradiation for producing crosslinked nitrile butadiene rubber/polyvinyl chloride raw rubber cots[J]. Journal of Radiation Research and Radiation Processing, 2021, 39(1): 010203. (in Chinese) |
| [38] |
LI Y L, ZHENG Y Y. Preparation and electrochemical properties of polyaniline/reduced graphene oxide composites[J]. Journal of Applied Polymer Science, 2018, 135(16): 46103. DOI:10.1002/app.46103 |
| [39] |
YANG Y J, HUANG H J. A polyaniline-modified electrode-based FIA system for sub-ppb-level chromium(VI) analysis[J]. Analytical Chemistry, 2001, 73(6): 1377-1381. DOI:10.1021/ac001252l |
| [40] |
麻丽峰. 电沉积回收模拟含重金属废水中重金属实验研究[D]. 天津: 天津大学, 2007. MA L F. Experimental study on recovery of heavy metals from simulated wastewater containing heavy metals by electrodeposition[D]. Tianjin: Tianjin University, 2007. (in Chinese) |
| [41] |
李若男, 张国凤, 陈舜胜. 纤维素纳米纤维基吸附剂的制备及水中重金属的去除[J]. 化工环保, 2022, 42(2): 195-202. LI R N, ZHANG G F, CHEN S S. Preparation of cellulose nanofiber-based adsorbent and removal of heavy metal from water[J]. Environmental Protection of Chemical Industry, 2022, 42(2): 195-202. (in Chinese) DOI:10.3969/j.issn.1006-1878.2022.02.012 |
| [42] |
CHARAZIŃSKA S, LOCHYŃSKI P, BURSZTA-ADAMIAK E. Removal of heavy metal ions form acidic electrolyte for stainless steel electropolishing via adsorption using Polish peats[J]. Journal of Water Process Engineering, 2021, 42: 102169. DOI:10.1016/j.jwpe.2021.102169 |
| [43] |
XIA L, FENG H, ZHANG Q P, et al. Centrifugal spinning of lignin amine/cellulose acetate nanofiber for heavy metal ion adsorption[J]. Fibers and Polymers, 2022, 23(1): 77-85. DOI:10.1007/s12221-021-3210-0 |
| [44] |
张胤杰, 易华炜, 谭笑, 等. 绿茶生物炭负载纳米零价铁对地下水中五价钒的去除效果及机理研究[J]. 北京化工大学学报(自然科学版), 2022, 49(2): 13-23. ZHANG Y J, YI H W, TAN X, et al. Removal and mechanism of pentavalent vanadium in groundwater by green tea biochar loaded with nano-zero-valent iron[J]. Journal of Beijing University of Chemical Technology (Natural Science), 2022, 49(2): 13-23. (in Chinese) |








