2. 昆明理工大学 复杂有色金属资源清洁利用国家重点实验室,昆明 650093;
3. 云南文山铝业有限公司,文山 663000
2. State Key Laboratory of Complex Nonferrous Metal Resources Clean Utilization, Kunming University of Science and Technology, Kunming 650093;
3. Yunnan Wenshan Aluminum Co., Ltd., Wenshan 663000, China
近年来,我国氧化铝产业发展迅速,氧化铝总产量已多年位居世界首位,2020年已达到7 313.2万吨,约占世界总产量的54.6%[1-2]。目前,世界上95%以上的氧化铝都是采用拜耳法工艺生产,其主要过程包括铝土矿高温高压溶出、赤泥沉降、晶种分解等工序[3]。在拜耳法生产氧化铝的过程中,有机物可通过多种途径进入拜耳循环,约96%的有机物来源于铝土矿,其余有机物来源于工序中添加的浮选剂、絮凝剂等物质[4]。我国的铝土矿主要以有机物含量高达0.05%~0.1%的一水硬铝石型为主[5-6],随着铝土矿的不断开发利用,其品位逐渐降低且有机物含量越来越高[7]。当有机物在拜耳液中不断循环累积达到一定浓度后,会给氧化铝的正常生产带来严重的危害,主要归纳为降低种分分解率、影响氧化铝的质量、改变溶出液的物化性质、增加碱耗及恶化生产环境等[8-10]。因此,去除拜耳液中的有机物对于氧化铝生产具有重要意义。
目前,脱除拜耳液中有机物的常规方法主要有铝土矿焙烧法、母液焙烧法、沉淀法、结晶法、吸附法、离子交换法及生物法等[11-17],这些方法存在能耗大、成本高、二次污染严重、可处理的有机物范围窄及沉淀剂用量大等问题。因此,寻找一种切实可行的方法来去除拜耳液中的有机物已成为我国氧化铝工业急需解决的重要课题。
高级氧化技术(advanced oxidation processes, AOPs)是Glaze等[18]在20世纪80年代提出的一种清洁环保的新型有机物处理工艺,该技术具有反应速率快、去污效率高、应用灵活、不产生二次污染等优点,在污水处理方面具有广阔的应用前景。本文概述了高级氧化技术的原理与特点,重点介绍了高级氧化技术在拜耳液中有机物去除方面的应用现状,总结了各高级氧化技术的优缺点并展望了其未来发展趋势,以期为相关研究提供参考。
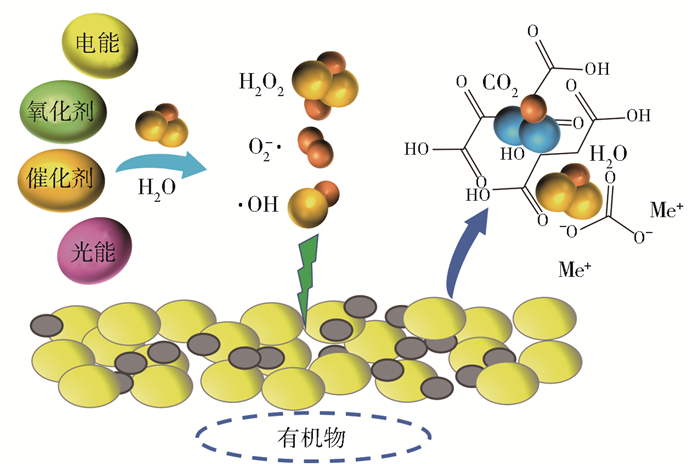
1 高级氧化技术的原理与特点 1.1 原理高级氧化技术的氧化机理如图 1所示。通过向反应体系中输入氧化剂(如O3和H2O2等)、催化剂(如镍铜合金、CuO、TiO2等)以及外界能量(如电能、光能等),产生高活性氧自由基(如·OH,O2-·,H2O2等),经过一系列亲电加成、电子转移及断键反应后,废水中的有机污染物被转化为小分子中间产物、CO2、H2O和无机盐等物质,从而实现有机废水的无害化处理[19-20]。其中,·OH的氧化能力极强且非常活泼,其氧化还原电位(E0)高达2.8 V[21],仅次于氟(E0=2.87 V),是O3(E0=2.07 V)的1.35倍[22],几乎能与所有的含氢化合物作用且无二次污染。
|
图 1 高级氧化技术的氧化机理示意图 Fig.1 Schematic illustration of the oxidation mechanism in AOPs |
高级氧化技术具有以下几方面的特点:(1)速度快、效率高。高级氧化技术在反应过程中可以产生较多·OH,其电子亲和能为569.3 kJ/mol,较强的电负性使其易于选择性作用于高电子云密度点,在高电子密度的有机物(如含硝基、磺酸基和氯基等基团的有机物)的氧化方面具有显著效果[23-24]。(2)可控性好。作为化学法处理有机物的途径之一,可以添加氧化剂和催化剂使链式反应不间断地运行,实现有机物的降解去除;通过控制反应条件和加入化学药剂可以随时控制链式反应进行及中止反应[25]。(3)适用范围广。高级氧化技术应用方便灵活,不仅可以单独用于有机物废水的预处理和深度处理,还可以与其他技术组合使用,通过不同高级氧化技术之间的相互强化作用,达到提高处理效率和降低成本的目的[26]。(4)节能环保。·OH作为高级氧化技术的中间产物,可引发后续链式反应[27]。仅需要在反应初始阶段以能量刺激产生大量·OH,而在反应进行过程中,链式反应自发放出的热量将为系统供能,直至链式反应终止[28]。同时,·OH能将有机物高效绿色降解,产物主要有小分子物质、CO2、H2O和无机盐等。
2 高级氧化技术去除拜耳液中有机物的研究现状目前已报道的用于去除拜耳液中有机物的高级氧化技术主要有臭氧氧化法(ozone oxidation, O3)、湿式氧化法(wet oxidation, WO)、光催化氧化法(photocatalytic oxidation, PCO)及复合高级氧化技术等。
2.1 臭氧氧化法O3是一种强氧化剂,E0高达2.07 V,由于其具有作用范围广、快速高效、无污染等优点而受到广泛关注。臭氧氧化法主要通过链式反应产生的·OH强烈氧化溶液中部分难降解的有机物而发挥作用,亦被广泛应用于杀菌消毒及水质脱色处理等方面,其链式反应过程如式(1)~(10)所示[29-31]。
| $ \mathrm{O}_{3}+\mathrm{OH}^{-} \rightarrow \mathrm{HO}_{2}^{-}+\mathrm{O}_{2} $ | (1) |
| $ \mathrm{O}_{3}+\mathrm{HO}_{2}^{-} \rightarrow \mathrm{HO}_{2} \cdot+\mathrm{O}_{3}^{-} \cdot $ | (2) |
| $ \mathrm{HO}_{2} \cdot \rightarrow \mathrm{O}_{2}^{-} \cdot+\mathrm{H}^{+} $ | (3) |
| $ \mathrm{O}_{2}^{-} \cdot+\mathrm{H}^{+} \rightarrow \mathrm{HO}_{2} \cdot $ | (4) |
| $ \mathrm{O}_{3}+\mathrm{O}_{2}^{-} \cdot \rightarrow \mathrm{O}_{3}^{-} \cdot+\mathrm{O}_{2} $ | (5) |
| $ \mathrm{O}_{3}^{-} \cdot+\mathrm{H}^{+} \rightarrow \mathrm{HO}_{3} \cdot $ | (6) |
| $ \mathrm{HO}_{3} \cdot \rightarrow \mathrm{O}_{3}^{-} \cdot+\mathrm{H}^{+} $ | (7) |
| $ \mathrm{HO}_{3} \cdot \rightarrow \cdot \mathrm{OH}^{-}+\mathrm{O}_{2} $ | (8) |
| $ \mathrm{HO}_{3} \cdot \rightarrow \cdot \mathrm{OH}^{-}+\mathrm{O}_{2} $ | (9) |
| $ \mathrm{HO}_{4} \cdot \rightarrow \mathrm{HO}_{2} \cdot+\mathrm{O}_{2} $ | (10) |
陈映等[32]研究了臭氧对铝酸钠溶液中有机物的氧化去除效果的影响,结果表明:臭氧对铝酸钠溶液中有机碳和还原性杂质的氧化效果明显,但是对于草酸钠的氧化效果并不突出;作为一种清洁氧化剂,臭氧在氧化去除有机物的同时并未向铝酸钠溶液中带入其他杂质。Hay[33]研究了臭氧氧化法去除拜耳液散发的独特异味,这种异味来源于铝土矿溶出过程中产生的挥发性低分子量有机物(如氨、乙醛和丙酮等),结果表明,臭氧氧化可除去臭味组成物中85%的有机物,净化效果显著。
臭氧氧化法处理拜耳液中部分有机物的效果显著,但是单一臭氧氧化对于草酸钠等有机物的去除效果并不明显,同时臭氧易降解含碳碳双键的有机物,生成醇、醛、酮、酸等小分子中间产物,但很难进一步将其矿化为二氧化碳[34]。此外,工艺成本高及O3制备效率低是限制该技术工业化应用的最大难题。因此,可以考虑臭氧联合其他高级氧化技术,在增强臭氧氧化效果的同时克服其不足之处,从而推进臭氧氧化法的工业化进程。
2.2 湿式氧化法强氧化物(空气、氧气等)在高温(150~350 ℃)、高压(0.5~20 MPa)下可产生大量·OH,湿式氧化法正是基于此特性,在液相水的存在下对溶液中的有机物进行高温高压氧化处理,将其高效氧化降解为CO2和H2O等小分子物质[35-36]。
Arnswald等[37]提出了通过管式消化器,在高温高压下向拜耳液中加入氧化物(如空气、氧气、臭氧等)来氧化其中的有机物,在处理过程中氧气含量须控制在1%(体积分数)以下,以避免达到爆炸极限。为了降低有机物氧化的难度,程芳燕等[38]利用H2O2通过湿式氧化法脱除铝酸钠溶液中的腐殖酸类有机物,在溶出温度为260 ℃、苛性碱的质量浓度为230 g/L、Al2O3质量浓度为110 g/L、碳碱质量浓度低于5 g/L、H2O2用量为80 mL/L的条件下,总碳量和草酸钠的去除率均大于45%。杜振华等[39]采用H2O2湿式氧化法脱除拜耳液中的有机物,考察了母液中苛性碱浓度、反应时间、反应温度和H2O2用量等关键因素对有机物去除效率的影响,结果表明,在苛性碱的质量浓度为280 g/L、H2O2用量为80 mL、反应温度为80 ℃的条件下,氧化反应进行2 h后,总有机物脱除率为60.86%,草酸钠脱除率达65.31%,对有机物的脱除效果显著。
近年来,关于催化湿式氧化法的报道越来越多,催化剂可以降低反应活化能,使得自由基的氧化能力大幅提升,从而提高有机物的去除效率,此外,催化剂的使用还可以提高氧化反应的安全性。目前,常用的催化剂主要是CuO、Cu2+和镍铜合金等。
Thé等[40]研究发现以镍铜合金作为催化剂,可以改善湿式氧化法面临的高温高压等苛刻条件,加速反应进程。Tardio等[41]研究了几种典型的催化剂(CuO、Fe2O3、Co3O4、Ni2O3和MnO2)在催化湿式氧化法去除铝酸钠溶液中有机物的效果,结果表明:催化剂的催化强化作用大小依次为:CuO > MnO2 > Co3O4 > 无催化剂 > Ni2O3 > Fe2O3;在强碱条件下,CuO具有更大的溶解度,故其催化效果突出;其他催化剂的效果不明显,原因是其在强碱溶液中很难溶解,并在后续氧化过程中消耗掉产生的自由基中间体,抑制氧化反应进行。同时,Tardio等还提出了CuO对铝酸钠溶液中丙二酸钠的催化机理:CuO通过配位反应溶解于铝酸钠溶液中,分解丙二酸过氧中间产物,反应产生具有更高活性的过氧中间体,从而促进了丙二酸钠氧化。Tardio等[42]使用湿式氧化法,以CuO作为催化剂处理拜耳液中的醋酸钠、草酸钠、丙二酸钠和琥珀酸钠等有机物,结果表明:当温度为165 ℃、氧气分压为0.5 MPa时,CuO在常规溶液中只能催化氧化丙二酸钠;而在高碱性拜耳液中,在同等条件下,CuO能使醋酸钠和琥珀酸钠均发生氧化,说明丙二酸钠在CuO催化氧化过程中发生了共氧化现象。Eyer等[43]使用湿式氧化法,以CuO为催化剂,在反应温度为165 ℃、氧气分压为0.5 MPa的条件下,将有机物中的丙二酸钠合成草酸钠和碳酸钠,结果发现,水合酮丙二酸是重要中间体,CuO使自由基的氧化活性大幅增强,可显著提升有机物的去除效率。Brown[44]研究了催化湿式氧化法在用于铝酸钠溶液中有机物氧化时的氢气生成问题,发现使用催化剂可以降低湿式氧化温度,同时减少爆炸性气体的生成。陈文汨等[45]使用湿式氧化法,以CuO为催化剂去除铝酸钠溶液中的有机物,结果表明:在反应温度为260 ℃、氧气分压为1 MPa、CuO添加量为5 g/L的条件下,当反应时间从1 h延长至3 h时,有机物转换率从86.2%提升到94.6%,草酸钠亦被完全分解;在无CuO催化剂的情况下,当反应时间从1 h延长到3 h时,有机物去除率从64.1%提升到79%。原因是CuO在特殊条件下可形成配合物以及氧化过程中发生自由基反应,可以使有机物更快、更彻底地分解。
与常规方法相比,湿式氧化法克服了适用范围窄、处理效率低、二次污染严重和氧化速率慢等缺点,但是仍需克服反应条件苛刻和一次性投资巨大等局限性。
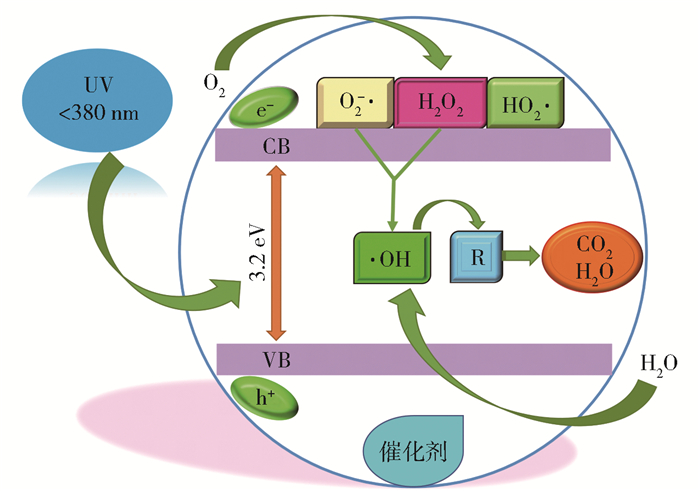
2.3 光催化氧化法光催化氧化法是利用催化剂,通过光激发引起氧化还原反应来氧化分解废水中污染物的方法,其原理如图 2所示。在常规条件下将光辐射和光敏催化剂(如TiO2、SnO2等)引入反应体系,催化剂吸收紫外光(UV)而发生能级跃迁,电子由低能价带(VB)跃迁至高能导带(CB)上,产生电子-空穴对(e--h+),与表面吸附的H2O和O2反应,产生氧化活性基团,如·OH、O2-·及HO2·等,进而高效氧化有机物(R)[46]。该方法可以避免湿式氧化法高温高压的苛刻条件,具有有机物去除效率高、反应条件要求低及反应速率快等优点,在有机废水处理领域应用广泛。
|
图 2 光催化氧化原理示意图 Fig.2 Schematic diagram showing the principle of photocatalytic oxidation |
李国庆[47]以SiO2/TiO2复合气凝胶为光催化剂,以拜耳液中的草酸钠、腐殖酸等有机物为对象,研究了光催化氧化法的氧化效果,结果表明,当光源功率为0.5 kW、外加氧化剂为H2O2(质量分数30%)、氧化剂添加量为6%(质量分数)、催化剂添加量为30 g/L和光源密度为3支/10 L时,光催化反应6 h后,有机物去除率达到52%。Pareek等[48-49]以工业TiO2为催化剂,在环形光反应器中研究了光对拜耳液中有机物的降解作用,结果显示:总有机碳(TOC)转化率与稀释比(V(水) ∶V(拜耳液))成反比,当稀释比为40 ∶1及催化剂用量为1 g/L时,105 min内可降解约30%的总有机碳;当稀释比为20 ∶1及催化剂用量为2 g/L时,反应2 h后,总有机碳的转化率提高至50%。
光催化氧化法具有反应性和化学稳定性高、毒性小、成本低等优点,能够有效处理拜耳液中的有机物。但是,为了最大化利用光能,仍需寻找溶液的最佳稀释比以及筛选和制备高效光催化剂。薄膜光反应器是一种将光催化剂作为特殊薄膜的反应器,具有成本低、催化剂易于分离及光利用率高等特点,是传统光反应器的良好替代品[50-51],但在催化剂薄膜的筛选及制备方面尚有待进一步深入研究。
2.4 复合高级氧化技术随着对于拜耳液中有机物成分的研究不断深入,单一高级氧化技术难以有效去除日益复杂的各种有机物。将多种高级氧化技术联用可达到“1+1 > 2”的效果,其相互之间的协同作用可有效提高·OH浓度,加快有机物的降解速率,降低高级氧化技术的应用成本。针对拜耳液中有机物的去除,目前仅研究了臭氧氧化法与H2O2湿式氧化法联用(O3/H2O2),H2O2与O3的反应过程包括O3和OH-反应生成HO2-,以及H2O2部分解离,并引发·OH氧化有机物,反应如式(11)~(13)所示[52]。
| $ \mathrm{O}_{3}+\mathrm{OH}^{-} \rightarrow \mathrm{HO}_{2}^{-}+\mathrm{O}_{2} $ | (11) |
| $ \mathrm{H}_{2} \mathrm{O}_{2}+\mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{HO}_{2}^{-}+\mathrm{H}_{3} \mathrm{O}^{+} $ | (12) |
| $ \mathrm{O}_{3}+\mathrm{HO}_{2}^{-} \rightarrow \cdot \mathrm{OH}+\mathrm{O}_{2}^{-} \cdot+\mathrm{O}_{2} $ | (13) |
Soplin等[53]比较了O3和O3/H2O2去除拜耳液中有机物的效果,评估了氧化剂浓度对有机物去除率的影响,结果表明:在O3质量浓度为21.9 mg/L及温度为80 ℃时,5 h后有机物的降解率仅为12%,进一步增加O3剂量并未提升降解效果,原因可能是O3的饱和位点数量有限;当O3质量浓度为21.9 mg/L、H2O2浓度为0.05 mol/L及温度为80 ℃时,5 h后有机物的降解率提高至19%,添加低浓度H2O2可改善臭氧氧化效果,加速反应动力学,提高·OH的产出效率;当O3质量浓度为21.9 mg/L,H2O2浓度为0.5 mol/L及温度为80 ℃时,5 h后有机物的降解率下降到15.6%,表明过量H2O2可能作为·OH螯合剂而干扰有机物降解。
O3与H2O2联用可有效解决单一高级氧化技术面临的种种缺陷,例如湿式氧化法面临的反应条件苛刻、设备材料要求高等问题以及臭氧氧化法面临的成本高昂等问题。
3 其他高级氧化技术在拜耳液中有机物处理方面的应用潜力除上述介绍的高级氧化技术外,还有其他高级氧化技术,主要包括过硫酸盐氧化法(persulphate oxidation, PSO)、电催化氧化法(electrocatalytic oxidation, EO)、超声氧化法(ultrasonic oxidation, US)、超临界水氧化法(supercritical water oxidation, SCWO)、芬顿氧化法(Fenton oxidation process, FOP)等,目前,这些氧化技术尚未应用于拜耳液中有机物的处理。垃圾渗滤液、部分有机废水与拜耳液含有相似的成分,如腐殖质、甲酸盐、乙酸盐、草酸盐、柠檬酸盐或芳香族化合物等,这些高级氧化技术已应用于垃圾渗滤液与部分有机废水的处理中,表明其具有应用于拜耳液中有机物去除的潜力。通过综述这些高级氧化技术的原理、特点及具体实例,旨在为今后拜耳液中有机物的去除提供更多的研究思路。
3.1 过硫酸盐氧化法过硫酸盐氧化法是近年来新出现的高级氧化技术。过硫酸盐在水中可电离出强氧化性的过硫酸根(S2O82-)(E0=2.01 V),与臭氧的氧化还原电位极为接近(E0=2.07 V)[54]。同时,过硫酸盐在光、电和热等能量的激发下可催化生成硫酸根自由基(SO4-·),其E0=2.5~3.1 V,甚至超过了·OH,在降解难处理的有机污染物方面表现出起效快、二次污染少等优势,能够快速高效地降解有机物[55]。与其他高级氧化技术相比,过硫酸盐氧化法的选择性更强,SO4-·可去除某些·OH无法处理的有机物。
娄晓祎[56]以水中的腐殖酸为模型污染物,研究了过硫酸盐对腐殖酸的氧化效果,结果表明:当过硫酸盐浓度低于7.5 mmol/L时,腐殖酸的降解效率随其升高而增大;当过硫酸盐浓度高于10 mmol/L时,腐殖酸的降解效率随其升高而减小,同时体系中存在的Cl-和Br-均可抑制腐殖酸降解,且Cl-的抑制效果明显弱于Br-;此外,该降解过程还可产生卤乙酸等有毒的卤代副产物。
在该技术的实际应用中,可以考虑使用物化沉淀或冷冻法高效除盐,在净化有机物的同时,避免二氯卤代污染物的产生,从而清洁高效地去除有机物。
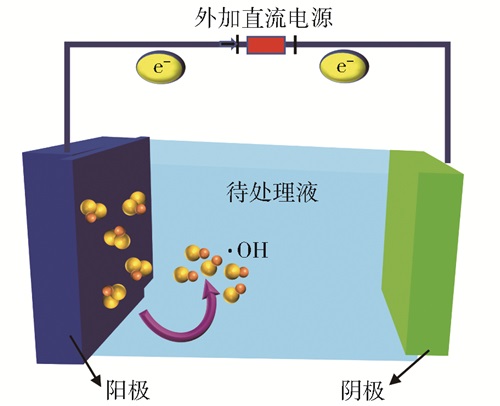
3.2 电催化氧化法电催化氧化法的原理是将处理液引入电解槽,在电流作用下,电极材料表面产生·OH等活性基团,使有机物氧化降解(图 3)。该方法具有氧化能力较强、物料投加量少及清洁环保等优点。
|
图 3 电催化氧化原理示意图 Fig.3 Schematic diagram showing the principle of electrocatalytic oxidation |
Fernandes等[57]采用硼掺杂金刚石、Ti/Pt/PbO2和Ti/Pt/SnO2·Sb2O4作为阳极材料,通过电化学氧化法处理垃圾渗滤液中的腐殖酸,结果表明:当电流密度为700 A/m2、Cl-质量浓度为2.5~4.5 g/L时,氧化8 h后,化学需氧量(COD)去除量大于2 g/L。该方法可消耗腐殖酸中的一部分配位基团,如醌基、酚基、芳香基和氢键等,使类腐殖物质的络合能力、芳香性和流动性降低,最终实现这类物质的降解。此外,据报道,铂阳极的电氧化体系也可以有效地氧化降解草酸盐[58]。
电催化氧化法在拜耳液中有机物去除方面具有潜在的应用价值。然而,该方法存在如下缺陷:处理有机污染物的浓度比较高,难以直接处理导电性较差的废水,受电极材料的限制较大且电耗较高。
3.3 超声氧化法超声氧化法可利用频率范围为16 kHz~1 MHz的超声波辐射溶液,在溶液中产生超声空化现象。空化气泡在极短时间和极小空间内溃灭时,可在局部形成高温(> 5 000 K)、高压(> 100 MPa)及超高含量的·OH和H2O2等强氧化性基团,为在常规条件下难降解的有机物提供特殊的氧化环境,使降解速率骤增。有机物的声分解去除可以通过其在空化气泡内热分解或者在本体溶液中受自由基攻击而实现,生成羟基化产物。第一种机制是非挥发性化合物的主要去除途径,第二种机制通常是挥发性污染物的降解途径。由水溶液声解产生的·OH可以在气相、气-液界面或溶液本体中重新组合而产生H2O2和水,如式(14)~(17)所示[59]。
| $ \mathrm{H}_{2} \mathrm{O} \rightarrow \cdot \mathrm{OH}+\mathrm{H} \cdot(\text {热分解}) $ | (14) |
| $ \cdot \mathrm{OH}+\mathrm{H} \cdot \rightarrow \mathrm{H}_{2} \mathrm{O} $ | (15) |
| $ 2 \cdot \mathrm{OH} \rightarrow \mathrm{H}_{2} \mathrm{O}_{2} $ | (16) |
| $ 2 \mathrm{H} \cdot \rightarrow \mathrm{H}_{2} $ | (17) |
然而,如果溶液被氧饱和,则H2O2和更多的·OH会在空化气泡中产生,并且在气-液界面或溶液本体中产生额外的H2O2,如式(18)~(21)所示。
| $ \mathrm{O}_{2} \cdot+\mathrm{H} \cdot \rightarrow \mathrm{HO}_{2} \cdot $ | (18) |
| $ \mathrm{O}_{2} \rightarrow \mathrm{O}+\mathrm{O} $ | (19) |
| $ \mathrm{O}+\mathrm{H}_{2} \mathrm{O} \rightarrow \cdot \mathrm{OH}+\cdot \mathrm{OH} $ | (20) |
| $ \mathrm{HO}_{2} \cdot+\mathrm{HO}_{2} \cdot \rightarrow \mathrm{H}_{2} \mathrm{O}_{2}+\mathrm{O}_{2} $ | (21) |
超声氧化法综合了自由基氧化、高温分解、超临界水氧化等技术优势,具有降解条件温和、效率高、适用范围广及无二次污染等特点,是一种很有发展潜力和应用前景的清洁水处理技术。
王松林[60]利用超声氧化法处理垃圾渗滤液中的COD,结果发现:COD去除率随着超声功率密度的增大、初始pH的增大及初始浓度的减小而增大;添加适量NaCl能够提高COD去除率,然而NaCl投入量存在极限值,过量反而使COD去除率下降;加入TiO2能够进一步提高COD的超声去除率。
超声氧化技术能够去除水中的某些有机污染物,但降解成本高、对亲水性和难挥发性有机物的处理效果较差以及对TOC去除不彻底等缺点极大地限制了其工业化应用,可以考虑超声氧化法联用其他高级氧化技术来处理难降解的有机物。
3.4 超临界水氧化法温度和压力明显高于临界温度(374.1 ℃)和临界压力(21.83 MPa)的均匀水相称为超临界水。超临界水氧化法利用超临界水作为介质,通过其中溶解的大量O2氧化分解溶液中的有机物质,使其快速转变为CO2和H2O[61]。超临界水具有不同于常规液体或气体的显著特征:密度接近液体,黏度接近气体,扩散系数大于液体且表面张力为零,介电常数急剧减小等[62-63]。基于超临界水能与非极性物质和其他有机物完全互溶的特性,强氧化性自由基在其中的传质效率极高,可快速地氧化降解有机物。
李巧丽[64]在连续管式反应器中,分别采用H2O2和CuSO4作为氧化剂及催化剂,通过超临界水催化氧化含有大量腐殖质、氨氮、重金属、氯代有机物和无机盐的垃圾渗滤液,结果发现:当温度为480 ℃、压力为28 MPa、过氧倍数为5时,处理10 min后,COD去除率为89.9%;当催化剂Cu2+的质量浓度为0.5 g/L时,有机物的降解效率可达96.2%。
处理效率高、清洁无污染和净化彻底等特性,使超临界水氧化技术在有机物处理方面具有巨大潜力。但目前仍然存在一些问题,例如设备易腐蚀、盐沉积现象频发、最佳反应条件及反应速率难以精确控制等。
3.5 芬顿氧化法19世纪80年代,法国化学家Fenton发现了芬顿氧化法。在酸性条件下,H2O2中引入Fe2+,可催化产生·OH,如式(22)所示[65]。
| $ \mathrm{Fe}^{2+}+\mathrm{H}_{2} \mathrm{O}_{2} \rightarrow \mathrm{Fe}^{3+}+\cdot \mathrm{OH}+\mathrm{OH}^{-} $ | (22) |
随后,Fe3+被H2O2还原成Fe2+和·OOH,实现Fe2+循环再生,保证反应可持续进行,如式(23)所示。
| $ \mathrm{Fe}^{3+}+\mathrm{H}_{2} \mathrm{O}_{2} \rightarrow \mathrm{Fe}^{2+}+\mathrm{H}^{+}+\cdot \mathrm{OOH} $ | (23) |
近年来,由于以Fe2+为催化剂的典型芬顿氧化法可产生大量难处理的铁泥并且氧化范围受限,已不能满足实际生产需要,故现在发展出以零价铁、铁盐或其他过渡金属(如Al、Ce、Cu、Mn、V等)替代Fe2+催化剂的类芬顿氧化法,可在一定程度上弥补典型芬顿氧化法的不足[66-68]。
聂玉伦[69]以FeOxH2x-3/Fe0为催化剂,利用类芬顿氧化法降解邻苯二甲酸二甲酯、2, 4-二氯苯氧乙酸和腐殖酸等难降解的有机物,结果表明:反应60 min后,邻苯二甲酸二甲酯被完全降解;反应20 min后,2, 4-二氯苯氧乙酸的降解率达到91.6%;反应90 min后,腐殖酸的TOC浓度与反应前相比下降了62%。上述结果表明芬顿氧化法更易使得芳香环裂解,可将原始有机物有效降解为小分子物质,废水的可生化性明显提高。
芬顿氧化法具有反应条件温和、操作简便、氧化效果显著及成本较低等优点,因此该方法在拜耳液中有机物处理方面具有很大的应用潜力。但在实际应用中存在Fe2+用量大、H2O2利用率不高以及反应环境(如pH)较苛刻等问题,限制了该方法的进一步广泛使用。
3.6 其他复合高级氧化技术近年来,利用其他复合高级氧化技术处理垃圾渗滤液、腐殖酸和乙酸等的研究较多。表 1描述了此类复合高级氧化技术的经典应用案例,总结了这些案例的最佳实验条件及主要结论,比较了各方法的优势与劣势,可以为拜耳液中有机物处理方面的研究提供一定的参考。
| 下载CSV 表 1 复合高级氧化技术在有机物处理中的应用 Table 1 Application of combined advanced oxidation processes in the treatment of organic matter |
高级氧化技术具有速度快、效率高、可控性好、适用范围广且环境友好等优势,在拜耳液中有机物去除方面具有广阔的应用前景。但是目前仍然存在较大的局限性,例如高耗能、高成本、对设备要求高等缺点。在拜耳液中复杂、难处理的有机物降解方面,高级氧化技术的未来发展趋势主要为:
(1) 继续深入开发复合高级氧化技术,通过不同高级氧化技术之间的协同作用,更加高效地产生强氧化性自由基,有效克服单一高级氧化技术的现有缺陷,提高有机物的处理效率和降低成本。
(2) 有机物的种类繁多,对于不同有机物的氧化降解机理需要进一步深入研究,以便“对症下药”,选择合适的氧化方法处理目标物。
(3) 研究成本更低、效果更好的新型氧化剂和催化剂,以有效增加自由基的产率,进一步提高有机物的去除效率。相信随着相关研究的不断深入,高级氧化技术将会取得较大进展,最终在成本效益和环境友好之间实现“双赢”。
| [1] |
罗林. 2020年全年中国氧化铝行业产量及出口贸易情况: 氧化铝累计产量突破7 000万吨[EB/OL]. [2021-03-26]. https://d.qianzhan.com/xnews/detail/541/210326-bfd897f5.html. LUO L. China's alumina industry output and export trade in 2020: the cumulative output of alumina exceeds 70 million tons[EB/OL]. [2021-03-26]. https://d.qianzhan.com/xnews/detail/541/210326-bfd897f5.html. (in Chinese) |
| [2] |
中国产业发展研究网. 2020年全球氧化铝产量达到1.34亿吨, 同比增长1.41%[EB/OL]. [2021-02-07]. http://www.chinaidr.com/tradenews/2021-02/167229.html. China Industrial Development Research Network. Global alumina production reaches 134 million tons in 2020, a year-on-year increase of 1.41%[EB/OL]. [2021-02-07]. http://www.chinaidr.com/tradenews/2021-02/167229.html. (in Chinese) |
| [3] |
周伟. 氧化(H2O2)去除铝酸钠溶液中的有机物及其对晶种分解的影响研究[D]. 贵阳: 贵州大学, 2016. ZHOU W. Removal of organic compounds from sodium aluminate solution by oxidation (H2O2) and its effect on seed decomposition of sodium aluminate solution[D]. Guiyang: Guizhou University, 2016. (in Chinese) |
| [4] |
POWER G P. The impact and control of organic compounds in the extraction of alumina from bauxite[C]//Proceedings of the 5th AusIMM Extractive Metallurgy Conference. Perth, 1991: 337-345.
|
| [5] |
赖智敏. 拜耳法生产氧化铝高压溶出过程有机物研究[J]. 中国金属通报, 2020(2): 108, 110. LAI Z M. Study on organic compounds in high pressure dissolution process of alumina production by Bayer process[J]. China Metal Bulletin, 2020(2): 108, 110. (in Chinese) DOI:10.3969/j.issn.1672-1667.2020.02.068 |
| [6] |
韩跃新, 柳晓, 何发钰, 等. 我国铝土矿资源及其选矿技术进展[J]. 矿产保护与利用, 2019, 39(4): 151-158. HAN Y X, LIU X, HE F Y, et al. Current situation of bauxite resource and its beneficiation technology in China[J]. Conservation and Utilization of Mineral Resources, 2019, 39(4): 151-158. (in Chinese) |
| [7] |
张涛, 俞小花, 彭建蓉, 等. 石灰拜耳法处理某铝土矿溶出性能的研究[J]. 昆明理工大学学报(自然科学版), 2017, 42(1): 9-13. ZHANG T, YU X H, PENG J R, et al. Study on dissolution performance of bauxite by lime Bayer process[J]. Journal of Kunming University of Science and Technology (Natural Science Edition), 2017, 42(1): 9-13. (in Chinese) |
| [8] |
SMEULDERS D E, WILSON M A, ARMSTRONG L. Poisoning of aluminum hydroxide precipitation by high-molecular-weight fractions of Bayer organics[J]. Industrial and Engineering Chemistry Research, 2001, 40(25): 5901-5907. DOI:10.1021/ie010216p |
| [9] |
POWER G, LOH J S C, VERNON C. Organic compounds in the processing of lateritic bauxites to alumina Part 2: effects of organics in the Bayer process[J]. Hydrometallurgy, 2012, 127-128: 125-149. DOI:10.1016/j.hydromet.2012.07.010 |
| [10] |
俞小花, 朱炳桥, 俞双林, 等. 氧化铝生产过程中有机物的影响与去除[J]. 矿产综合利用, 2020(2): 16-22. YU X H, ZHU B Q, YU S L, et al. Influence and removal method of organics in the process of alumina production[J]. Multipurpose Utilization of Mineral Resources, 2020(2): 16-22. (in Chinese) DOI:10.3969/j.issn.1000-6532.2020.02.003 |
| [11] |
陈文汨, 陈学刚. 焙烧氧化法在去除拜耳法有机物中的应用(下)[J]. 轻金属, 2008(9): 13-16. CHEN W M, CHEN X G. The application of calcination oxidation on organics removal in Bayer process (Part B)[J]. Light Metals, 2008(9): 13-16. (in Chinese) |
| [12] |
PULPEIRO J G F, GAYOL M, BOILY H, et al. A year of operation of the solid-liquid calcination (SLC) process[M]//DONALDSON D, RAAHAUGE B E. Essential readings in light metals. Cham: Springer, 2016: 309-313.
|
| [13] |
赵瑜, 刘桂华, 皮溅清. 铝酸钠溶液中草酸钠的石灰苛化[J]. 世界有色金属, 2013(11): 76-77. ZHAO Y, LIU G H, PI J Q. Lime causticization of sodium oxalate in sodium aluminate solution[J]. World Nonferrous Metals, 2013(11): 76-77. (in Chinese) |
| [14] |
袁艺, 陈义. 铝酸钠溶液中有机物排除试验研究[J]. 广州化工, 2014, 42(5): 59-60, 78. YUAN Y, CHEN Y. Experimental study on the organic compounds removal in sodium aluminate solution[J]. Guangzhou Chemical Industry, 2014, 42(5): 59-60, 78. (in Chinese) DOI:10.3969/j.issn.1001-9677.2014.05.022 |
| [15] |
ZAYTSEV Y A, LANKIN V P, LIPIN V A, et al. Some capabilities of removal of organic substances from Australian Bayer process liquors[M]//GRANDFIELD J. Light metals. 129th ed. Hoboken: John Wiley & Sons, Inc., 2000: 59-64.
|
| [16] |
ATKINS P, GROCOTT S. The liquid anion exchange process for organics removal[M]//GRANDFIELD J. Light metals. 122nd ed. Hoboken: John Wiley & Sons, Inc., 1993: 151-157.
|
| [17] |
MOHOTTIGE T N W, GINIGE M P, KAKSONEN A H, et al. Bioelectrochemical oxidation of organics by alkali-halotolerant anodophilic biofilm under nitrogen-deficient, alkaline and saline conditions[J]. Bioresource Technology, 2017, 245(Part A): 890-898. |
| [18] |
GLAZE W H, KANG J W, CHAPIN D H. The chemistry of water treatment processes involving ozone, hydrogen peroxide and ultraviolet radiation[J]. Ozone: Science & Engineering, 1987, 9(4): 335-352. |
| [19] |
许青, 杜俊琪, 刘伟, 等. 高级氧化和脱吸耦合处理地下污水工艺的研究[J]. 北京化工大学学报(自然科学版), 2013, 40(3): 79-83. XU Q, DU J Q, LIU W, et al. The combination of advanced oxidation and desorption to treat polluted underground water[J]. Journal of Beijing University of Chemical Technology (Natural Science), 2013, 40(3): 79-83. (in Chinese) DOI:10.3969/j.issn.1671-4628.2013.03.015 |
| [20] |
赵丽红, 聂飞. 水处理高级氧化技术研究进展[J]. 科学技术与工程, 2019, 19(10): 1-9. ZHAO L H, NIE F. Research progress in advanced oxidation technology for water treatment[J]. Science Technology and Engineering, 2019, 19(10): 1-9. (in Chinese) DOI:10.3969/j.issn.1671-1815.2019.10.001 |
| [21] |
孙怡, 于利亮, 黄浩斌, 等. 高级氧化技术处理难降解有机废水的研发趋势及实用化进展[J]. 化工学报, 2017, 68(5): 1743-1756. SUN Y, YU L L, HUANG H B, et al. Research trend and practical development of advanced oxidation process on degradation of recalcitrant organic wastewater[J]. CIESC Journal, 2017, 68(5): 1743-1756. (in Chinese) |
| [22] |
赵霞, BAKHROM I, 李亚斌, 等. 污水高级氧化技术的研究现状及其新进展[J]. 水处理技术, 2018, 44(4): 7-10, 16. ZHAO X, BAKHROM I, LI Y B, et al. Research status and new progress of advanced oxidation technology for wastewater treatment[J]. Technology of Water Treatment, 2018, 44(4): 7-10, 16. (in Chinese) |
| [23] |
DINÇ Ö, ERSOY Z G, ÖZTVRK H, et al. Determination of operating conditions for hydrogen peroxide and hydroxyl radical production in electro-peroxone process[J]. Celal Bayar University Journal of Science, 2019, 15(3): 235-239. |
| [24] |
LUCAS M S, PERES J A, LI P G. Advanced oxidation processes for water and wastewater treatment[J]. Water, 2021, 13(9): 1309. DOI:10.3390/w13091309 |
| [25] |
ROÉ-SOSA A, AMABILIS-SOSA L E, REYES-PRADO M A, et al. Potential reuse of wastewater containing recalcitrant organic compounds, treated by advanced oxidation processes[J]. Integrated Environmental Assessment and Management, 2021, 17(3): 651-653. |
| [26] |
ZHANG M H, GAO D W. Microwave-enhanced advanced oxidation process of biogas slurry from cow manure anaerobic digester[J]. Environmental Technology, 2021, 42(12): 1846-1852. DOI:10.1080/09593330.2019.1682060 |
| [27] |
ALIASGHARLOU N, BAHRAM M, ZOLFAGHARI P, et al. Modeling and optimization of simultaneous degradation of rhodamine B and acid red 14 binary solution by homogeneous Fenton reaction: a chemometrics approach[J]. Turkish Journal of Chemistry, 2020, 44(4): 987-1001. DOI:10.3906/kim-2002-59 |
| [28] |
LINCHO J, GOMES J, MARTINS R C. Paraben compounds-part Ⅱ: an overview of advanced oxidation processes for their degradation[J]. Applied Sciences, 2021, 11(8): 3556. DOI:10.3390/app11083556 |
| [29] |
LÓPEZ-VINENT N, CRUZ-ALCALDE A, GANIYU S O, et al. Coagulation-flocculation followed by catalytic ozonation processes for enhanced primary treatment during wet weather conditions[J]. Journal of Environmental Management, 2021, 283: 111975. DOI:10.1016/j.jenvman.2021.111975 |
| [30] |
PASTOR M A S, BOTELHO JUNIOR A B, ESPINOSA D C R, et al. Application of advanced oxidation process using ozonation assisted with hydrogen peroxide for organic compounds removal from Bayer liquor[J/OL]. Ozone: Science & Engineering, 2021. [2021-05-18]. https://doi.org/10.1080/01919512.2021.1924118.
|
| [31] |
HEKMATSHOAR R, KHORAMNEJADIAN S, ALAHABADI A, et al. Potential of ammonium chloride-activated carbon for decomposition of penicillin G by catalytic ozonation process (COP)[J]. International Journal of Environmental Science and Technology, 2022, 19: 1131-1138. DOI:10.1007/s13762-021-03180-x |
| [32] |
陈映, 朱杨昆, 段昌祥, 等. 臭氧氧化拜耳法铝酸钠溶液中有机物的试验研究[J]. 云南冶金, 2018, 47(1): 81-85. CHEN Y, ZHU Y K, DUAN C X, et al. The experimental study on organic matter in sodium aluminate solution used in ozonation Bayer process[J]. Yunnan Metallurgy, 2018, 47(1): 81-85. (in Chinese) DOI:10.3969/j.issn.1006-0308.2018.01.018 |
| [33] |
HAY P S. Removal of odorous materials from Bayer process condensate[C]//Chemeca 2010: Engineering at the Edge. Adelaide, 2010: 2153-2162.
|
| [34] |
陈湘清, 陈金洲, 熊道陵, 等. 拜耳法生产氧化铝中有机物脱除研究进展[J]. 轻金属, 2014(9): 23-28. CHEN X Q, CHEN J Z, XIONG D L, et al. Research progress of removing organic in Bayer process of aluminum production[J]. Light Metals, 2014(9): 23-28. (in Chinese) |
| [35] |
毛兵, 陶海祥, 贾军芳, 等. 微波催化湿式氧化法处理含酚废水的研究[J]. 染料与染色, 2021, 58(2): 55-58, 41. MAO B, TAO H X, JIA J F, et al. Study on microwave catalytic wet air oxidation for phenol-containing wastewater[J]. Dyestuffs and Coloration, 2021, 58(2): 55-58, 41. (in Chinese) |
| [36] |
MAREE Z, STRYDOM C A, BUNT J R. Chemical and physical characterization of spent coffee ground biochar treated by a wet oxidation method for the production of a coke substitute[J]. Waste Management, 2020, 113: 422-429. DOI:10.1016/j.wasman.2020.06.025 |
| [37] |
ARNSWALD D W, KALTENBERG H G, GUHL E. Removal of organic carbon from Bayer liquor by wet oxidation in tube digesters[M]//DONALDSON D, RAAHAUGE B E. Essential readings in light metals. Cham: Springer, 2016: 304-308.
|
| [38] |
程芳燕, 金会心, 李洋, 等. H2O2去除铝酸钠溶液中腐殖酸类有机物的实验研究[J]. 过程工程学报, 2016, 16(6): 927-932. CHENG F Y, JIN H X, LI Y, et al. Experimental study on removal of humic acid organics from sodium aluminate solution by H2O2 oxidation[J]. The Chinese Journal of Process Engineering, 2016, 16(6): 927-932. (in Chinese) |
| [39] |
杜振华, 李军旗, 金会心, 等. H2O2湿式氧化法脱除铝酸钠溶液中的有机物[J]. 湿法冶金, 2014, 33(6): 483-486. DU Z H, LI J Q, JIN H X, et al. Removal of organics from industrial sodium aluminate solution by hydrogen peroxide wet oxidation[J]. Hydrometallurgy of China, 2014, 33(6): 483-486. (in Chinese) |
| [40] |
THÉ P, WILLIAMS F, GUTHRIE J. Mass transfer studies on wet oxidation of Bayer liquor: pilot plant evaluation[M]//GRANDFIELD J. Light metals. Hoboken: John Wiley & Sons, Inc., 1985: 103-116.
|
| [41] |
TARDIO J, BHARGAVA S, PRASAD J, et al. Catalytic wet oxidation of the sodium salts of citric, lactic, malic and tartaric acids in highly alkaline, high ionic strength solution[J]. Topics in Catalysis, 2005, 33(1-4): 193-199. DOI:10.1007/s11244-005-2527-z |
| [42] |
TARDIO J, BHARGAVA S, EYER S, et al. Interactions between specific organic compounds during catalytic wet oxidation of Bayer liquor[J]. Industrial & Engineering Chemistry Research, 2004, 43(4): 847-851. |
| [43] |
EYER S, BHARGAVA S, TARDIO J, et al. Selective organic removal from the alumina industrial liquor: wet oxidation and catalytic wet oxidation of disodium malonate[J]. Industrial & Engineering Chemistry Research, 2002, 41(5): 1166-1170. |
| [44] |
BROWN N. Kinetics of copper-catalysed oxidation of Bayer liquor organics[M]//GRANDFIELD J. Light metals. Hoboken: John Wiley & Sons, Inc., 1989: 121-130.
|
| [45] |
陈文汨, 张浩. 湿式氧化法去除铝酸钠溶液中有机物的研究[J]. 湖南有色金属, 2011, 27(5): 35-37, 74. CHEN W M, ZHANG H. Study on romoval of organics from Bayer liquor by wet oxidation[J]. Hunan Nonferrous Metals, 2011, 27(5): 35-37, 74. (in Chinese) DOI:10.3969/j.issn.1003-5540.2011.05.010 |
| [46] |
ZHU L L, AWAIS M, JAVED H M A, et al. Photo-catalytic pretreatment of biomass for anaerobic digestion using visible light and Nickle oxide (NiOx) nanoparticles prepared by sol gel method[J]. Renewable Energy, 2020, 154: 128-135. DOI:10.1016/j.renene.2020.02.119 |
| [47] |
李国庆. 无机钛源TiO2、TiO2/SiO2气凝胶的制备表征及光催化去除拜耳液中有机物的研究[D]. 昆明: 云南大学, 2019. LI G Q. Preparation of TiO2、TiO2/SiO2 aerogels and photocatalytic removal of organic compounds in Bayer liquor[D]. Kunming: Yunnan University, 2019. (in Chinese) |
| [48] |
PAREEK V, BRUNGS M P, ADESINA A A. Photocausticization of spent Bayer liquor: a pilot-scale study[J]. Advances in Environmental Research, 2003, 7(2): 411-420. DOI:10.1016/S1093-0191(02)00013-8 |
| [49] |
PAREEK V K, BRUNGS M P, ADESINA A A. Continuous process for photodegradation of industrial Bayer liquor[J]. Industrial & Engineering Chemistry Research, 2001, 40(23): 5120-5125. |
| [50] |
朱哲欣, 叶美英. 微流控芯片中TiO2薄膜的低温制备[J]. 硅酸盐通报, 2017, 36(7): 2397-2403. ZHU Z X, YE M Y. Low temperature preparation of titanium dioxide thin films in microfluidic chip[J]. Bulletin of the Chinese Ceramic Society, 2017, 36(7): 2397-2403. (in Chinese) |
| [51] |
全洪新, 徐莫临. 水热合成二氧化钛薄膜及光催化反应器的研究[J]. 辽宁化工, 2018, 47(10): 996-998. QUAN H X, XU M L. Hydrothermal synthesis of titanium dioxide film and photocatalytic reactor[J]. Liaoning Chemical Industry, 2018, 47(10): 996-998. (in Chinese) DOI:10.3969/j.issn.1004-0935.2018.10.006 |
| [52] |
彭人勇, 杨秀娟. O3/H2O2处理嘧啶废水的研究[J]. 环境工程学报, 2011, 5(3): 601-604. PENG R Y, YANG X J. Study on treatment of wastewater containing pyrimidine by O3/H2O2[J]. Chinese Journal of Environmental Engineering, 2011, 5(3): 601-604. (in Chinese) |
| [53] |
SOPLIN M A, BOTELHO JUNIOR A B, BALTAZAR M P G, et al. Application of advanced oxidative process for organic compounds removal from Bayer liquor[M]//TOMSETT A. Light metals. Cham: Springer, 2020: 60-64.
|
| [54] |
LEE Y C, LO S L, CHIUEH P T, et al. Microwave-hydrothermal decomposition of perfluorooctanoic acid in water by iron-activated persulfate oxidation[J]. Water Research, 2010, 44(3): 886-892. DOI:10.1016/j.watres.2009.09.055 |
| [55] |
NETA P, HUIE R E, ROSS A B. Rate constants for reactions of inorganic radicals in aqueous solution[J]. Journal of Physical and Chemical Reference Data, 1988, 17(3): 1027-1284. DOI:10.1063/1.555808 |
| [56] |
娄晓祎. 无机阴离子活化过硫酸盐氧化降解典型有机污染物的研究[D]. 上海: 东华大学, 2016. LOU X Y. Inorganic anions mediated persulfate activation for degradation of typical organic pollutants in wastewater[D]. Shanghai: Donghua University, 2016. (in Chinese) |
| [57] |
FERNANDES A, SANTOS D, PACHECO M J, et al. Electrochemical oxidation of humic acid and sanitary landfill leachate: influence of anode material, chloride concentration and current density[J]. Science of the Total Environment, 2016, 541: 282-291. DOI:10.1016/j.scitotenv.2015.09.052 |
| [58] |
LI S, VAN DER EST A, BUNCE N J. Electrochemical oxidation of oxalate ion in the presence of fluoride ion, and radical analysis by ESR[J]. Electrochimica Acta, 2009, 54(13): 3589-3593. DOI:10.1016/j.electacta.2009.01.025 |
| [59] |
INCE N H, TEZCANLI G, BELEN R K, et al. Ultrasound as a catalyzer of aqueous reaction systems: the state of the art and environmental applications[J]. Applied Catalysis B: Environmental, 2001, 29(3): 167-176. DOI:10.1016/S0926-3373(00)00224-1 |
| [60] |
王松林. 超声处理垃圾渗沥液及有机污染物的研究[D]. 武汉: 华中科技大学, 2006. WANG S L. Study on treatment of landfill leachate and organic pollutants by ultrasonic irradiation[D]. Wuhan: Huazhong University of Science and Technology, 2006. (in Chinese) |
| [61] |
OSHIMA Y, HAYASHI R, YAMAMOTO K. Pilot-scale laboratory waste treatment by supercritical water oxidation[J]. Environmental Sciences, 2006, 13(4): 213-218. |
| [62] |
FERREIRA-SANTOS P, ZANUSO E, GENISHEVA Z, et al. Green and sustainable valorization of bioactive phenolic compounds from Pinus by-products[J]. Molecules, 2020, 25(12): 2931. DOI:10.3390/molecules25122931 |
| [63] |
BRUNNER G. Near critical and supercritical water. Part I. hydrolytic and hydrothermal processes[J]. The Journal of Supercritical Fluids, 2009, 47(3): 373-381. DOI:10.1016/j.supflu.2008.09.002 |
| [64] |
李巧丽. 超临界水氧化法处理垃圾渗滤液[D]. 太原: 太原理工大学, 2013. LI Q L. Supercritical water oxidation of landfill leachate[D]. Taiyuan: Taiyuan University of Technology, 2013. (in Chinese) |
| [65] |
王磊. 基于芬顿反应的单晶SiC化学机械抛光液研究[D]. 广州: 广东工业大学, 2015. WANG L. Research for chemical mechanical polishing solution based on Fenton reaction for single crystal SiC[J]. Guangzhou: Guangdong University of Technology, 2015. (in Chinese) |
| [66] |
BABUPONNUSAMI A, MUTHUKUMAR K. A review on Fenton and improvements to the Fenton process for wastewater treatment[J]. Journal of Environmental Chemical Engineering, 2014, 2(1): 557-572. DOI:10.1016/j.jece.2013.10.011 |
| [67] |
WANG N N, ZHENG T, ZHANG G S, et al. A review on Fenton-like processes for organic wastewater treatment[J]. Journal of Environmental Chemical Engineering, 2016, 4(1): 762-787. DOI:10.1016/j.jece.2015.12.016 |
| [68] |
BOKARE A D, CHOI W. Review of iron-free Fenton-like systems for activating H2O2 in advanced oxidation processes[J]. Journal of Hazardous Materials, 2014, 275: 121-135. DOI:10.1016/j.jhazmat.2014.04.054 |
| [69] |
聂玉伦. 多相芬顿催化剂及其催化降解有机污染物机制的研究[D]. 北京: 中国科学院生态环境研究中心, 2008. NIE Y L. Heterogeneous Fenton catalysts and the mechanism of catalytic degradation of organic pollutants[D]. Beijing: Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, 2008. (in Chinese) |
| [70] |
ATMACA E. Treatment of landfill leachate by using electro-Fenton method[J]. Journal of Hazardous Materials, 2009, 163: 109-114. DOI:10.1016/j.jhazmat.2008.06.067 |
| [71] |
王春霞, 肖书虎, 赵旭, 等. 光电芬顿氧化法深度处理垃圾渗滤液研究[J]. 环境工程学报, 2009, 3(1): 11-16. WANG C X, XIAO S H, ZHAO X, et al. Study on the treatment of landfill leachate by photo-electro-Fenton oxidation[J]. Chinese Journal of Environmental Engineering, 2009, 3(1): 11-16. (in Chinese) |
| [72] |
MO J, JIANG J C, PENG L, et al. Study on degradation of humic acids by UV/O3/H2O2 process[J]. Fresenius Environmental Bulletin, 2015, 24(6): 2017-2025. |
| [73] |
CUI M, JANG M, CHO S H, et al. Enhancement in mineralization of a number of natural refractory organic compounds by the combined process of sonolysis and ozonolysis (US/O3)[J]. Ultrasonics Sonochemistry, 2011, 18(3): 773-780. DOI:10.1016/j.ultsonch.2010.11.009 |
| [74] |
潘留明, 季民, 王秀朵, 等. TiO2纳米管/UV/O3对腐殖酸的降解及应用基础[J]. 天津大学学报, 2010, 43(4): 333-338. PAN L M, JI M, WANG X D, et al. Degradation and applied basis of humic acid treated by TiO2 nanotubes/UV/O3[J]. Journal of Tianjin University, 2010, 43(4): 333-338. (in Chinese) |
| [75] |
康春莉, 唐晓剑, 郭平, 等. UV/O3法降解乙酸的影响因素[J]. 吉林大学学报(理学版), 2008, 46(1): 162-165. KANG C L, TANG X J, GUO P, et al. Influencing factors of photodegradation of acetic acid by UV/O3 processes[J]. Journal of Jilin University(Science Edition), 2008, 46(1): 162-165. (in Chinese) DOI:10.3321/j.issn:1671-5489.2008.01.036 |
| [76] |
柴斯琦, 杨汉培, 高照, 等. 自掺杂型BiOBr光催化剂-过硫酸盐协同体系可见光降解腐殖酸的研究[J]. 环境科技, 2019, 32(6): 54-59, 63. CHAI S Q, YANG H P, GAO Z, et al. Synergistic system of self-doping BiOBr photocatalyst with persulfate and their visible photocatalytic degradation of humic acid[J]. Environmental Science and Technology, 2019, 32(6): 54-59, 63. (in Chinese) DOI:10.3969/j.issn.1674-4829.2019.06.010 |
| [77] |
周宁. 超声/过硫酸盐法去除水中卡马西平及腐殖酸的研究[D]. 武汉: 华中科技大学, 2015. ZHOU N. Study on the degradation of carbamazepine and humic acid in water using ultrasonic combined with persulfate method[D]. Wuhan: Huazhong University of Science and Technology, 2015. (in Chinese) |
| [78] |
李前锋. 超声电化学活化过硫酸盐去除水中阿莫西林和腐殖酸的研究[D]. 武汉: 华中科技大学, 2016. LI Q F. Study on the removal of amoxicillin and humic acid by sono-electro-activated persulfate oxidation[D]. Wuhan: Huazhong University of Science and Technology, 2016. (in Chinese) |








