能源是社会生存与发展的基础,渗透到人类生活的每个角落。当前世界范围内,以煤炭和石油为主的化石能源仍然占据能源主体地位。然而,现有的能源利用方式存在许多问题,例如利用效率低下、温室气体排放产生温室效应、燃烧造成环境污染等。为保障人类社会的可持续发展,寻找低碳排放甚至无碳排放的高效洁净能源至关重要。氢能资源丰富、方便易得、无碳排放,具有传统化石能源无法比拟的优势,将在能源领域发挥重要作用。氢气的储存是氢经济中非常重要的一环[1-2],人们已经开发了多种氢气储存技术,例如高压储氢、液态储氢、固态储氢、液相有机氢载体储氢等,但迄今为止,能够规模化应用的技术不多,并且都存在各种问题。
高压储氢是目前多数燃料电池汽车企业优选的储氢方式,如日本丰田公司的“未来(Mirai)”燃料电池车采用70 MPa的高压储氢罐[3],通用公司的“氢能-3”燃料电池车亦然,在该压力下携带3.1 kg氢,可以行驶270 km。遗憾的是,目前中国还没有完全掌握这种技术,并且推广高压氢气储罐需要面对较大的社会压力。此外,高压储氢对钢制材料的要求较高,还要避免氢溢出和氢脆现象[4]。液态储氢(这里特指降温氢气液化储氢)是太空运载、国防等特殊领域沿用已久的成熟技术,但因其存在能耗过大、气化率高以及安全性问题,目前尚未应用于民用市场[5]。固态储氢一直是相关研究领域的热点,但实用化案例仍然较少,LaNi5系材料是一个较为成功的案例,可应用于镍氢电池车[6-7]。除金属储氢[8]外,固态储氢领域还发展了碳质储氢材料(包括活性炭、富勒烯、碳纳米管等)[9]、无机离子型化合物储氢材料(如NaAlH4、LiBH4等)[10]、有机金属框架材料(MOFs)[11-12]等方向,但受制于成本、可逆特性、稳定性、大规模生产等因素,这些材料都未能实现工业化应用。另外,固态储氢的一大问题是难以与现有的基础设施相契合,其大规模应用受限[13]。
液相有机氢载体(或有机液体化合物储氢材料)(liquid organic hydrogen carriers,LOHCs)的概念在20世纪70—80年代被提出[14],其思路可概括为通过不饱和有机物和氢气反应,将氢能储存在加氢产物中,在释能阶段通过脱氢反应放出氢气以实现氢能利用。这一思路的最大优势体现在储氢形式和安全性上,因为LOHCs的性质和燃料油类似,其在储存、运输、维护、保养方面安全方便,通过对已有的基础设施进行适当调整即可满足储氢和输运的需求[15]。
从以上不同储氢技术的对比中可以看出,工业应用对储氢材料的要求大致包括:易活化,单位质量、单位体积的储氢含量高;具有高度反应可逆性,可在近常温、常压下进行;具有良好的循环寿命和稳定性;吸收、离解氢过程中的平衡氢压小,即滞后效应小;具有优良的抗毒性能,不易受外部气体侵害;成本较低;对环境和生物无毒害;与现有基础设施相匹配等。
目前还没有任何一种储氢介质可以满足上述所有条件,解决储氢材料适用性问题的关键在于匹配不同的使用场景。粗略地看,除航空航天和一些特种国防需求外,氢能使用终端大致可分为固定源用氢和交通运输用氢。前者强调大容量,后者强调大的储氢密度和运输的便利性。换言之,不同使用场景对储氢材料的上述要求的优先级并不相同。在多种储氢技术中,LOHCs的储氢密度高,应用安全、高效、环保、经济性高,可实现大规模、远距离存储和运输氢气[13],尤其是可适配现有能量输运设施(输油管线、罐车、油品库、加油站、燃油车油箱等)或者仅需对其进行适当改装,因此受到了广泛关注。本文综述了LOHCs的原理、材料和相关催化剂的研究进展,并通过工业应用案例讨论了LOHCs的应用前景和技术难点,为相关研究提供参考。
1 LOHCs的储氢原理与技术要求LOHCs通过对不饱和有机物加氢使其成为存储氢气的媒介,然后通过脱氢反应释放氢气以供后续单元使用[16]。LOHCs的储氢、释氢过程如图 1所示。

|
图 1 LOHCs的储氢、释氢过程 Fig.1 Storage and release of H2 by LOHCs |
一般情况下,氢气通过催化加氢(通常需要催化剂,在高温和中高压条件下进行,该反应一般是一个强放热反应)使不饱和LOHCs(记作H0-LOHCs)加氢,得到的饱和LOHCs材料(记作Hn-LOHCs,n表示1分子LOHCs中所加氢原子的个数)即可用于输送和储能,在使用端经催化脱氢(催化剂多为负载型贵金属,在一定的温度下进行),释放出的氢气可用于燃料电池或其他装置。理论上讲,含有不饱和键的有机物都可以作为储氢介质,但受储氢量、安全性、可重复性等指标的限制,现有常用的LOHCs材料主要包括碳环类芳烃、具有共轭结构的杂环化合物、甲醇和甲酸等。总的来说,以交通运输为目的的LOHCs材料需满足以下要求:1)无毒安全;2)熔点低,避免在常温下固化而引入溶剂;3)沸点高,避免高温脱氢反应下产物氢气不纯;4)储氢密度高,我国车用储氢气罐对储氢密度的要求为6.8%(质量分数,下同)[17],美国能源部对轻型车辆车载氢气的存储密度的技术目标为4.5%(或0.03 kg/L,2020年)、5.5%(或0.04 kg/L,2025年)和6.5%(或0.05 kg/L,最终目标)[18];5)与现有基础设施匹配;6)黏度较低,这对在低温地区使用尤其重要;7)反应焓变较小,避免造成脱氢时能量的浪费;8)工作温度适宜,如美国能源部对工作环境温度的技术目标为-40~60 ℃[18];9)较高的可重复性,可循环次数达1 500次[18];10)环保且廉价易得;11)较高的稳定性,对储存和使用设备没有腐蚀性;12)在催化脱氢范畴内,还应满足:放氢温度较低,有一定的放氢速率,不易使催化剂积碳失活,反应具有较高的选择性。
遗憾的是,目前尚未有任何一种LOHCs材料满足上述所有标准,但已有一些LOHCs材料可以有条件地满足上述要求,尤其是在一些关键指标上表现优异,如在储氢密度方面已能和液态储氢技术一争高下[19],因此LOHCs材料具有重大的应用潜力,部分材料甚至已有应用。
2 LOHCs材料正处于研究或已经商用的LOHCs材料包括甲苯[20]、萘[21]、苄基甲苯(MBT)[22]、二苄基甲苯(DBT)[23]、芴[24]、联苯[25]、二苯甲烷[26]、N-乙基咔唑(NEC)[27]、碱金属咔唑[28]、吲哚[29-30]、喹啉[31]、吩嗪[32]、苯酚钠[33]、氨硼烷[34]或N-杂碳硼烷[27]、甲醇[35-36]、甲酸[27]、氨基乙醇[37]以及上述物质的某些同系物等,这些物质粗略地可分为碳环化合物、杂环化合物[38]和其他物质。这三类化合物的理化性质区别较大,所需储运体系也不尽相同,本文仅列举研究较多且具有代表性的几种物质[28, 33, 39-41],目的是说明其理化特征性质,阐述其应用潜力,具体如表 1所示。
| 下载CSV 表 1 典型LOHCs材料及其理化性质 Table 1 Typical LOHCs molecules and their physiochemical properties |
在上述LOHCs化合物中,二苄基甲苯、甲苯和N-乙基咔唑已有商业应用的报道(见第4节);萘的储氢密度较高且研究广泛;吩嗪的稳定性高且原料可由生物质提供;甲醇的储氢密度极高,是液相储氢材料的明星分子;咔唑锂、苯酚钠等离子化合物相比于普通环状化合物脱氢反应焓较低。这些LOHCs分子在不同的方面具有一定的代表性。本文主要讨论的LOHCs主要以为移动源供氢为目的,由表 1可知,上述物质的储氢密度均较高,接近或达到美国能源部提出的6.5%的要求,都具有工业应用潜力。需要指出的是,除了咔唑、吩嗪、吲哚等含N杂环外,吡咯、咪唑、吡啶等的同系物也有研究[40],性质与之较为类似,在此不再详述。而含O或S等其他元素的杂环在LOHCs的应用中非常少见[42],这主要是加氢/脱氢选择性或催化剂毒化的问题所致[43]。
储氢量并非是衡量LOHCs材料的唯一指标(见第1节)。Niermann等[40]从能耗、脱氢温度、成本、材料性质、毒性与安全性、氢气流速几个方面对不同LOHCs分子进行了讨论,结果表明,二苄基甲苯、N-乙基咔唑和吩嗪可以在体系仍是液态时实现催化脱氢,产物氢气较为纯净,其中,二苄基甲苯和N-乙基咔唑的熔点不太高,易于以液态形式运输。甲醇在其他多个层面上都有一定的优势,但甲醇脱氢本身会产生CO2、CO、H2O,这既与碳减排的目的相悖(除非可以实现高效CO2捕集或是将甲醇脱氢产生的CO2全部分离储存,但以目前的技术水平都很难达到),也会带来装置成本的升高。事实上,甲醇脱氢本身也是催化研究的热点,相信如果CO2的问题得以解决,甲醇将是非常理想的储氢材料[36]。甲基环己烷(甲苯的全加氢产物)的起燃点低(需要额外的安全措施),萘和吩嗪的熔点较高(需要加入溶剂使体系为液态,但会导致储氢密度降低,且可能影响产物纯度),这些问题难以解决,只能增加装置成本,降低储运效率。综合上述特征以及蒸气压、毒性和生物降解性等因素,二苄基甲苯和N-乙基咔唑是目前最有工业应用潜力的LOHCs分子。二苄基甲苯更低的成本决定了其更适合应用于大宗氢气储运,N-乙基咔唑更低的脱氢温度及更快的释氢速率使其在为燃料电池运输工具供氢方面更具优势。
总的来说,不同指标对不同场景下的LOHCs储能材料有不同程度的影响。仍需指出,虽然没有任何一种代表性材料可以完美地满足所有要求,但这些要求本身的权重不同,决定了我们仍可以优选出特定场景下适用的LOHCs材料。考虑到新能源建设的社会价值和经济价值,LOHCs材料的选取最应注重的是储能效率、脱氢温度、是否适配现有技术、节能环保这几个指标,这些指标对应了储氢质量密度、催化剂与脱氢反应条件、黏度、熔沸点、毒性和反应焓变、碳足迹等参数。在其他指标如成本上,似乎甲苯、甲醇等大宗化学品拥有极大的优势,但这些化学品的低价也恰恰是由其大宗的性质决定的,一旦某种LOHCs材料得以量产,其价格势必会有所降低。此外,考虑到LOHCs本身在储运氢气的过程中几乎不产生消耗[44],不应过于重视LOHCs原料本身的价格,从经济的角度更应考虑LOHCs与现有基础设施的适配程度以及能量密度等因素。
3 LOHCs催化剂与催化装置如前所述,LOHCs的脱氢过程往往是吸热的,而加氢过程虽然是放热的,但一般也在高温下进行,催化剂的使用会大大降低加氢/脱氢过程的难度,通常使用多相催化剂,因为这有利于产物与催化剂的分离[45]。一般来说,这些催化剂多为负载型贵金属催化剂或类Raney Ni型过渡金属催化剂。同大多数催化材料一样,LOHCs相关的催化剂研究也集中于贵金属用量、几何效应与电子效应、分散度与载体结构等方面,本节主要讨论含N杂环类LOHCs(以N-乙基咔唑为代表)加氢与脱氢反应的催化剂和催化过程,兼谈碳环类LOHCs(以甲苯和二苄基甲苯为例)与杂环类LOHCs的催化剂的共性和特性。需要指出的是,甲醇、甲酸等非芳香性化合物的催化剂已有丰富的综述类文献对其进行讨论,这些催化剂与上述两种LOHCs的催化剂区别较大,此外,制约甲醇作为储氢分子商用的核心因素并非催化剂(见第2节),本节中不做讨论。
在杂环类化合物中,N-乙基咔唑是最有潜力的一类LOHCs分子。而在碳环LOHCs化合物中,苄基甲苯及二苄基甲苯具有较大的商业化潜力,但其脱氢温度较高,难以为交通工具上的燃料电池供氢。这两类LOHCs的储氢、释氢过程如图 2所示。
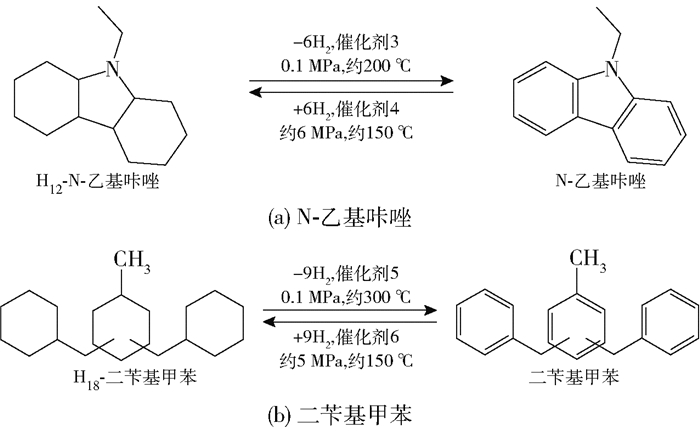
|
图 2 N-乙基咔唑和二苄基甲苯的储氢、释氢过程 Fig.2 Storage and release of H2 by N-ethylcarbazole and dibenzyltoluene |
从服务于氢燃料电池的LOHCs的使用方式来看,催化脱氢过程集成在运输工具中,脱氢反应吸热且催化剂在较高的温度下使用,对催化剂和催化装置的要求较高;而加氢过程往往在生产氢气的工厂中进行,规模较大,且化学品加氢过程的相关催化剂比较成熟。因此这里首先讨论脱氢催化剂。
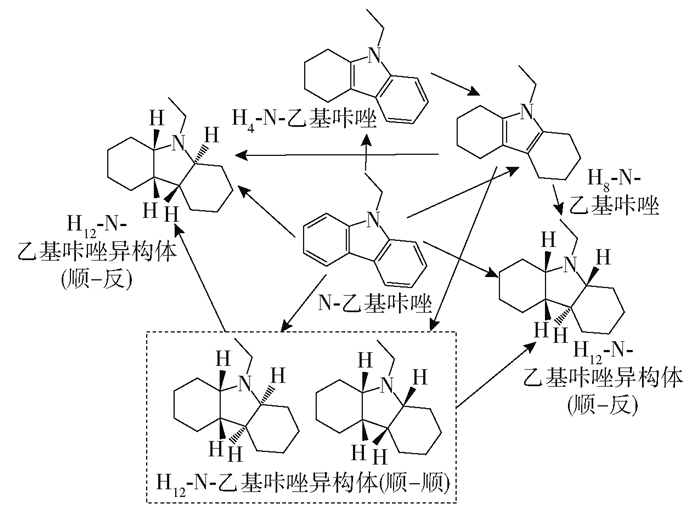
以N-乙基咔唑为代表的含N杂环类LOHCs的脱氢反应通常使用贵金属催化剂,其中以Pd为主要的活性组分。Yang等[46]对比了以Al2O3为载体的4种商业化负载型贵金属催化剂对全氢N-乙基咔唑(H12-NEC)的催化脱氢活性,结果表明,在180 ℃下,不同贵金属催化剂的催化性能大小顺序为:Pd>Pt>Ru>Rh。其中,在实验条件下,仅有Pd和Pt可以满足完全脱氢以及对NEC的选择性为100%的条件。Wang等[47]研究了以还原氧化石墨烯(rGO)为载体的多种贵金属,结果表明,不同贵金属催化H12-NEC脱氢的性能大小顺序为:Pd>Pt>Rh>Ru>Au,与Yang等[46]的研究结果基本相符。从上述研究可以看出,Pd是NEC等含N杂环LOHCs材料催化脱氢的最有潜力的活性组分。值得一提的是,Yang等[46]的研究表明,Rh/Al2O3催化此反应的活性较低,但产物分布中H4-NEC(脱除4分子H2的H12-NEC)的比例较高。需要指出,因NEC的熔点较高,在常温下通常呈固态,不利于存储和置换,保存一部分未完全脱氢的Hm-NEC对维持该体系为液态有利,这一点对NEC的实际应用有一定的意义,但这显然会降低LOHCs材料整体的有效储氢密度。
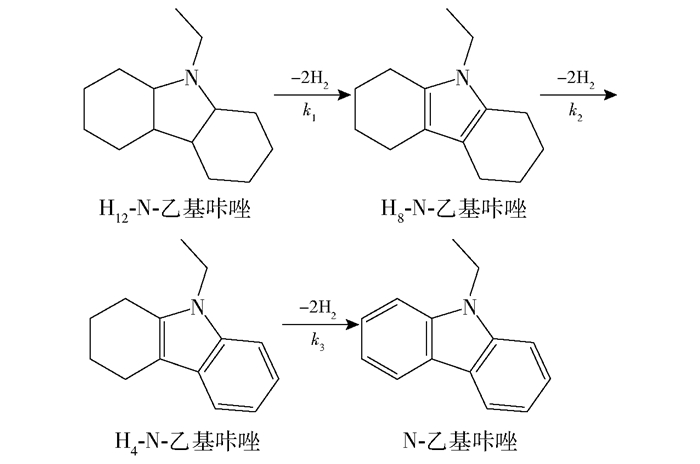
不完全脱氢的产物分布与不同脱氢产物的动力学性质有关。研究表明,H12-NEC催化脱氢分三步进行[48],如图 3所示。在脱氢过程中,含氮五元环上的2分子氢气率先脱除,然后是其中一个六元环,最终完全脱除生成NEC。3个反应通常都表现为一级反应,通过测算脱氢过程开始后不同时间的产物分布,可以计算出三步脱氢的动力学常数k1、k2、k3。例如,在180 ℃、101 kPa下,5%(质量分数,下同) Pd/Al2O3催化上述三步反应的动力学常数分别为:k1=0.321 min-1、k2=0.187 min-1、k3=0.002 298 min-1,k3与k1、k2的差距悬殊,表明H4-NEC为此反应的动力学稳定产物[46]。升高温度可以加速反应的进行,使得反应更加完全,这也提示了在实际应用中可以通过控温的方式调控H12-NEC的释氢速率及程度。类似地,NEC的同系物,如N-丙基咔唑(NPC)、N-丁基咔唑(NBC)等同样可用作LOHCs材料,其脱氢过程也分为类似图 3的三步反应,且H4-NPC脱氢生成NPC的活化能最高,为整体反应的决速步骤[49]。显然,随着N-取代基的增长,材料的分子量增大,而共轭环上储存氢气分子的量不变,导致整体的储氢密度降低。但是,这些取代基更长的N-烷基咔唑往往具有其他的优势,例如,在类似的条件下,NPC脱氢和加氢较NEC更为容易[49-50],且NPC的熔点更低,对于储运更具优势[51]。
通过动力学研究可以探索调控LOHCs释氢的方式[52-53],而针对活性位点的研究则可以优化催化剂,这一点对LOHCs的商业化应用同样至关重要。研究表明,作为目前效率最高的脱氢催化剂,Pd催化Hn-NEC脱氢反应具有明显的结构敏感性。例如,Sotoodeh等[54]通过在SiO2载体上调控Pd的载量得到不同粒径的Pd纳米粒子,经对比发现,平均粒径约为9.1 nm的4% Pd/SiO2的活性最高;经密度泛函理论(DFT)计算[54-55],还发现Hn-NEC在Pd表面的吸附需要多个位点协同作用,同样提示了Pd表面几何结构对反应性能的影响,而k3较小导致反应不完全的原因则与H8-及H4-NEC在催化剂表面的吸附较H12-NEC更强有关。Pt催化剂也表现出了类似的性质,实验表明,NEC在较大的Pt粒子(2~4 nm)表面脱氢有利,而在具有高缺陷含量的小颗粒(1~2 nm)表面反而容易发生脱烷基的副反应[56]。事实上,尺寸效应的本质即是不同大小的纳米粒子表面结构的差异带来的几何效应或与之相关的电子效应。通过合成暴露不同晶面的纳米粒子可以降低研究几何效应的复杂度。Wang等[57]合成了暴露不同晶面的Pd纳米粒子并将其负载于还原氧化石墨烯表面,测试其催化氢化N-乙基咔唑的脱氢反应性能,结果表明,Pd(100)晶面是Pd催化该反应的优势晶面,同时再次证明了H4-NEC脱氢生成NEC是该反应的决速步骤。
另外,关于NEC作为LOHCs的研究尚有几点与该物质本征特性相关的结论值得强调。NEC具有较高的储氢密度,事实上,虽然其储氢能力仅来源于咔唑的共轭π-结构,但N位及其链接的乙基仍至关重要。相较于芴,咔唑脱氢的难度明显降低(这也是杂环芳香化合物应用于车用LOHCs的潜力较大的重要原因),而乙基的引入不仅可以大幅降低咔唑的熔点,也可以在一定程度上提升LOHCs的催化脱氢活性(在相同条件下,N-乙基咔唑催化脱氢的速率是咔唑的3倍);同时,乙基还可以削弱N原子的孤对电子对催化剂活性位点的毒化作用[24, 48, 55-56, 58]。这些结论不仅提供了改善LOHCs分子综合性能的思路,也提示了催化剂高选择性的必要性,尤其是抑制N-侧链的催化断裂的重要性[56]。另外,Hn-NEC的异构现象值得关注,不同异构体的H12-NEC和中间产物的脱氢速率不同,一般而言,处于顺位的氢原子的脱氢速率较高[59]。
这些基础研究提示了优化LOHCs材料脱氢催化剂的思路,即调节其活性位点在催化过程中的几何效应和电子效应。针对几何效应,主要通过优化活性组分的颗粒粒径来调节,这一点在上文中已有描述,可以通过改变活性组分的载量实现;此外,根据其他领域金属催化剂的研究,也可以通过改变合成和处理条件来调节这一性能[60-62]。而针对电子效应,则主要通过对活性组分或载体进行调节和修饰来实现,以下列举两种常见的思路。
(1) 调节脱氢催化剂活性组分的电子结构可以通过合金化的方式实现,这种方式往往还可以降低贵金属的用量。仍以NEC为例,Jiang等[63]发现在Pd/SiO2催化剂中引入Cu或Ni可以同时提升H12-NEC的脱氢转化率和选择性,使催化剂在180 ℃下即显示出高催化性能。另外,Ni的引入同样有利于提升N-丙基咔唑的脱氢性能[64]。Wang等[65]在Pd/rGO催化剂中引入Cu,可以在保障催化剂性能的基础上显著降低Pd的用量,但过多的Cu会使Pd的电子向Cu迁移,从而降低催化剂的活性。而引入Au则可大幅提升催化性能,使催化反应的转化率和选择性均达到100%的时间缩短43%[66]。有趣的是,实验和理论计算的证据表明,这些合金化的策略同样改变了催化剂活性组分的粒径或分散度[67],事实上,几何效应和电子效应本来就是催化研究中相互影响的两个方面,不能孤立而谈,在催化理论研究中需要同时考虑、辩证对待。Kustov等[68]证明了Pt和Ru引入后Pd/TiO2催化剂的性能提升,值得一提的是,该文献还指出,微波参与可使脱氢过程更加高效。
(2) 贵金属催化H12-NEC脱氢还表现出明显的载体效应。例如,Gong等[69]在TiO2载体表面负载1%(质量分数,下同)的Pt或Pd,其性能即优于5%的Pd/Al2O3商用催化剂,结合X-射线衍射(XRD)、X-射线光电子能谱(XPS)、高分辨透射电子显微镜(HRTEM)、程序升温还原(TPR)等表征分析手段,发现金属-载体强相互作用(SMSI)对催化剂活性有重要的促进作用。Jiang等[70]发现在180 ℃下,不同贵金属负载于TiO2的催化性能大小顺序为:Pt/TiO2> Pd/TiO2>Rh/TiO2>Au/TiO2>Ru/TiO2。此外,Jiang等[71]认为,提升脱氢催化剂选择性的关键之一是降低催化剂表面的酸强度。除可还原性金属氧化物外,很多新型载体也显示出一定的应用潜力,例如金属有机框架[72]、碳纳米管[73]等。
甲苯、苄基甲苯、二苄基甲苯等碳环类LOHCs材料常用Pt作为脱氢催化剂的活性组分[74]。苄基甲苯和二苄基甲苯的沸点较高且较稳定,具有很好的应用前景,二者都是工业应用的导热油,其性质略有差别。碳环类LOHCs材料的脱氢温度高,蒸气压更低的二苄基甲苯在产物氢气的纯度方面更具优势;但苄基甲苯的黏度低,在低温下更易操作[75],使用二者的混合体系是平衡二者优劣势的有效思路[76]。另外需要指出,由于苄基在甲苯中的取代位置不固定,工业用苄基甲苯和二苄基甲苯都是多种异构体的混合物,在评价其加氢/脱氢活性时,常引入加氢度(DOH)和脱氢度(DOD)的概念,并且全氢-苄基甲苯或全氢-二苄基甲苯的脱氢遵循分步脱氢的机理,产物分布较为复杂,相比于色谱、质谱、核磁等方法,使用密度、折光率等指标表征DOH和DOD具有一定优势[77]。Modisha等[78]对比了不同贵金属催化全氢二苄基甲苯(H18-DBT)脱氢的性能,结果表明,Pt/Al2O3适合此反应,而Pd、Pd-Pt合金的活性均较差,反应在290~320 ℃的范围内进行,除产氢外,反应还会产生一定量的副产物甲烷。
除H18-DBT外,甲基环己烷也是常见的碳环类LOHCs材料,反应同样使用Pt作为催化剂(1% Pt/γ-Al2O3),在较高的温度(340~380 ℃)下进行,通常会产生副产物甲烷和苯[79]。日本千代田公司使用Pt/Al2O3催化甲基环己烷脱氢,目前已商业化应用(详见4.1节),催化剂为负载型的Pt颗粒,粒径约1 nm[80]。需要指出,该公司发现,通过对Pt/Al2O3催化剂预硫化,可以抑制上述副反应,防止甲基环己烷分解,该催化剂在低于400 ℃的条件下可使用10 000 h,转化率>95%,对甲苯的选择性>99%。Auer等[81]使用CO吸附的原位漫反射红外光谱等手段证明了对Pt/Al2O3催化剂预硫化可毒化台阶位的Pt,从而提高对产物的选择性。一些非贵金属也显示出一定的催化性能,例如Ni或Ni-Cu合金对苯、甲苯及萘的体系,但整体表现不如贵金属[82]。
针对碳环类LOHCs脱氢催化剂的改性思路与杂环类相似,多为引入其他元素或利用载体效应。例如,Pt-Re合金催化甲基环己烷脱氢的稳定性比Pt催化剂更高[74];掺入Mg[83]或S[84]也会提升Pt基催化剂的脱氢性能,且S元素的引入对反应的选择性也有好处,这可能和某些在Pt台阶位上的强吸附S物种有关。碳环类LOHCs脱氢催化剂的载体效应也非常明显,例如,在相同条件下Pt/CeO2较Pt/Al2O3的H18-DBT催化脱氢性能更高[85]。Aakko-Saksa等[86]发现,与NEC脱氢类似,载体的晶相对于H18-DBT的脱氢也有影响,在调节Pt/TiO2载体晶相的过程中,当载体为金红石-锐钛矿复合晶相时,催化剂的脱氢性能最优,经对比推测这可能和催化剂中Pt的粒径和催化剂表面的Lewis酸性有关。Shi等[87]系统对比了DBT催化加氢和脱氢过程中催化剂的载体效应,结果表明,当活性组分同为Pt时,脱氢反应活性的大小顺序为:Al2O3≈C>SBA-15>羟基磷灰石(HAP),加氢反应活性的大小顺序为:Al2O3>SBA-15>HAP>C,总体上Pt/Al2O3的表现最优。苄基甲苯和二苄基甲苯的催化反应条件和催化剂大同小异,贵金属的种类、载量、载体种类对反应速率都有影响,H12-MBT较H18-DBT的脱氢速率更快[22]。
3.2 加氢催化剂无论是杂环还是碳环类LOHCs材料,加氢催化剂仍主要以贵金属为主,尤其是Ru在绝大多数体系中显示出了优异的催化性能。例如,在5.16% Ru/γ-Al2O3存在时,在140 ℃、6.0 MPa压力下,NEC即可顺利加氢,转化率为100%,催化剂对H12-NEC的选择性为98%[88]。Eblagon等[89-90]、Ye等[91]及Wan等[92]比较了多种贵金属催化NEC加氢反应的性能,发现其活性大小顺序为:Ru>Pd>Pt>Ni,其中Ni为单质和负载型,贵金属均为单质。值得一提的是,Eblagon等[89, 93]还比较了催化过程中加氢产物的立体选择性,结果表明,Ru不仅展现出了更优的活性,其催化产物中全顺式H12-NEC的含量也最高。Eblagon等[93]指出,随NEC加氢程度的提升,不同异构化的加氢产物构成加氢反应网络,而不同的H12-NEC异构体之间也会相互转变,如图 4所示,顺式Hn-NEC更有利于进行脱氢反应。另外,需要指出,反式产物的热力学稳定性更高,故需要通过控制动力学来获得更高的立体选择性[93]。Eblagon等[93]还比较了不同商用贵金属催化剂在该反应网络中的表观速率常数,发现贵金属的种类对反应活性和选择性有决定性的影响。此外,加氢催化剂也显示出明显的载体效应,对5% Ru催化剂而言,Al2O3和TiO2是比较优秀的载体[93],并且疏水载体更有利于顺式产物的生成。
Fei等[94]观察到了加氢过程中的载体效应,例如介孔MoO3负载的Pd催化剂催化NEC加氢的性能较Pd/Al2O3更高,这是由于Pd-MoO3界面的氢溢流现象促进了HxMoO3相形成,进而促进反应快速进行。类似地,WO3负载的Ru催化剂同样存在显著的氢溢流现象,使其催化N-丙基咔唑加氢的性能较Ru/WO3大幅提升[95]。Yu等[96]在研究中指出,TiO2晶相对于Ru-Ni双金属体系催化NEC加氢的性能至关重要,与单一TiO2晶相作为载体的催化剂相比,负载于具有锐钛矿和金红石复合晶相的P25氧化钛载体上的贵金属具有更高的性能和应用潜力。使用稀土氢化物YH3作为载体的Ru/YH3催化剂的加氢条件极为温和,温度低至90 ℃,压力为1 MPa,对全顺式H12-NEC产物的选择性更是达到惊人的100%。除Y外,La和Gd的氢化物也显示出对杂环类LOHCs加氢的高催化活性[97]。
关于贵金属催化加氢的几何效应,Eblagon等[98]通过实验和计算证明,NEC的加氢反应首先发生在Ru的平台位,但由于位阻原因,加氢中间产物的进一步反应往往需要在较高的指数位点上进行。
前已述及,碳环类LOHCs材料的加氢和杂环类相似。仍以DBT为例,除Ru基催化剂外,Rh、Pt、Pd等贵金属和Raney Ni催化剂的应用都有文献报道[99-102],其中,Ru、Rh通常在低于220 ℃时即可催化反应进行,而Pt、Pd等则在高于220 ℃时更具优势,在某些情况下,Ni也表现出较高的加氢性能[99]。与杂环类相似,DBT的加氢过程同样是按环分步进行的,且遵循side-side-middle (SSM)机理,即两侧苄基先加氢,中间甲苯环后加氢[100-101]。MBT与之类似,加氢时一个苯环完全饱和后,另一个苯环才加氢[102]。
另外,通过将加氢和脱氢的活性组分整合到同一载体上,研究者设计了LOHCs加氢/脱氢双功能催化剂(通常是双金属)。例如,Zhu等[103]设计了Ru-Pd催化剂、Xue等[104]设计了Pd-Rh催化剂用于Hn-NEC体系的加氢-脱氢反应;而Shi等[87]则发现Pt/Al2O3可用作Hn-DBT体系的双功能催化剂。需要指出,仅从储运类储氢材料的定义来看,对于任何LOHCs材料,在大多数使用场景下,其加氢和脱氢的催化过程几乎不可能在同一空间进行,否则就失去了“储运”的意义,而任一功能失活的双功能催化剂也即随之失活,这样反而会造成贵金属资源的浪费。双功能催化剂对LOHCs材料的应用意义或许会体现在更加优异的性能、更加低廉的价格或是更加特殊的使用场景方面。
3.3 脱氢催化反应器面向应用的催化体系研究同样应该关注反应器的设计,LOHCs在制氢工厂中进行大宗加氢,反应工艺比较成熟,但针对车载燃料电池用氢的脱氢催化剂,需要考虑其在高空速等极端条件下的催化性能。在目前的研究中,常见的催化剂评价装置是间歇式反应器[85],即将Hn-LOHCs材料与催化剂置于反应器(通常是三颈烧瓶)中,在加热回流的条件下通入惰性气体,每隔一段时间取样,用色谱法测量反应过程中的产物分布。这种反应器可以方便地测算不同反应时间的反应体系状态,从而得出催化剂的动力学性质。但是,为了模拟在车用装置中的脱氢反应,评价往往在固定床反应器中进行,LOHCs分子直接泵送至高温催化剂中,再利用色谱法测量通过催化剂的产物分布。这种模式显然更加符合实际应用的需求,从而能更好地反映LOHCs在线脱氢的效果。
除了上述两种典型的反应器外,近年来还有新型反应器的报道。例如一种径向反应器[105],Hn-LOHCs从该反应器的中间进入,沿径向向外辐射并与催化剂床层反应。Modisha等[106]综述了目前常见的多种LOHCs在不同反应器中的反应条件与性能,指出反应装置的结构对反应性能有较大影响,提示传热传质引起的扩散性质对Hn-LOHCs脱氢反应的贡献。Shukla等[107]归纳了不同类型脱氢装置的优势与不足,指出虽然间歇式反应器的转化率高,但由于固定床反应器显然更能适配连续生产的场景,具有难以取代的优势。基于类似思路的多相干湿体系或脉冲喷雾系统、整体式催化剂系统、微反应器、膜反应器等各具优势,且普遍可以提高反应物的使用效率,但其设计往往更加复杂,在工业化过程中需进一步考虑工程因素。此外,在适配燃料电池时,还应考虑脱氢装置整体的可控性、产氢纯度等要求,必要时应加装缓冲区、原料或产物纯化装置等[108-109]。
3.4 小结总的来说,LOHCs材料的脱氢/加氢过程普遍仍需依赖贵金属材料,N-杂环类LOHCs脱氢反应的活性组分通常是Pd,碳环类LOHCs脱氢的活性组分通常是Pt,而催化这些材料进行加氢反应的最优活性组分通常是Ru。载体方面,一般使用比表面积较大的Al2O3或活性炭,但碳纳米管、孔材料、稀土材料等新型载体也有文献报道[70-73, 94-97]。对于催化剂的优化改性,可从改变活性组分的粒径分布、调节金属与载体的相互作用以及引入新组分(形成合金或硫化处理等)的角度考虑实现,其中第VIIIB族贵金属和La族稀土元素可能是活性组分和载体的优势元素,而低周期过渡金属和一些主族元素可能作为改性元素用于调节催化剂的几何效应与电子效应。从催化装置和催化剂应用放大的层面考虑,无论是碳环化合物还是杂环化合物,催化剂材料应相对简单,其脱氢过程应使用固定床催化装置或类似结构的反应器(尤其是车用装置),反应装置和催化剂放大/修饰应考虑相应的工程因素。需要指出的是,目前所用的贵金属催化剂中贵金属含量(质量分数通常≥1%)仍过高,为了降低成本,降低催化剂中贵金属用量至关重要。如果参照汽油车尾气处理三效催化剂中贵金属的含量(质量分数通常约为0.1%),或可保障LOHCs储氢技术的竞争力。
4 商用LOHCs的效率和技术难度 4.1 商用LOHCs材料综上所述,N-乙基咔唑和二苄基甲苯及其同系物是目前交通运输领域中使用LOHCs型储氢和供能物质的最优选择。事实上,这几种物质也是目前为数不多的LOHCs商业化案例中所使用的物质。例如,德国Hydrogenious Technologies公司[23]和H2-Industries公司[110]主要使用二苄基甲苯的异构体作为LOHCs材料,用于较大容量的氢气储运,而二苄基甲苯本身即是工业上常用的导热油,且成本较低,所以和基础设施的适配性较好,大容量和较为稳定的使用场景使其克服了释氢速率较慢的缺陷。武汉氢阳能源有限公司[111-112]主要关注氢能在氢动力汽车上的储存和应用,该公司采用了以含氮杂环化合物为主体的多种LOHCs材料的混合模式,可以在较低的温度(约200 ℃)下快速释放氢气。此外,该公司还发展了以LOHCs材料为介质的氢能源汽车,提示了这一思路用于整体设计解决交通工具储氢问题的可行性。日本千代田公司的SPERAHydrogen技术[20]使用甲苯作为LOHCs材料,以Pt基材料为脱氢催化剂,建设了包括位于Negara Brunei Darussalam的加氢工厂和位于日本川崎沿海地区的脱氢工厂的全球氢供应链示范工厂。氢气在文莱采购,并在环境温度和压力下以液态形式(即甲基环己烷)通过船舶运输到日本川崎。然后,从液体中提取氢气并将其提供给消费者。可以看出,这一方案同样关注于氢气的运输,尤其是长距离运输,而非氢气在交通工具上的释放。
4.2 LOHCs材料的循环性能、储能效率及经济性除了催化剂和反应装置的工程设计外,面向工业应用的LOHCs材料还应考虑其循环性能、储能效率及经济性等因素,这里做一简要讨论。
第1节已经提到,对于储氢材料,吸放氢循环性能是重要的工业指标。目前已有针对LOHCs多次储放氢性能的报道,但关于长周期循环试验的报道较少。Ali等[113]研究了NEC 3个周期的储放氢过程,结果表明,3个周期后,NEC释氢体积仍能基本达到理论值,表明NEC具有一定的循环性能。叶旭峰等[114]研究了NEC的4个储释氢周期,发现在循环数增加的过程中,加氢和脱氢速率同比不断变慢,说明催化剂在使用过程中不断失活,但产物中副产物不多,即NEC的循环性能尚可。NPC的循环性能与之类似,仍观察到前几个周期的储氢性能略有降低,但5个周期后储氢能力基本稳定[49]。DBT等碳环类LOHCs表现出同样优异的循环性能,但同样存在催化剂活性降低的现象[115]。Jorschick等[116]进一步研究了DBT经过405 h、13次的储放氢过程,结果表明,催化剂在前3~5个循环后活性明显下降,且产物中有少量副产物,约96 h后副产物量约为1.6%(质量分数);此外,作者还研究了不同循环过程对其储放氢性能的影响,发现更短的脱氢过程和更长的加氢过程对DBT和催化剂的稳定性都有好处。提升循环测试的苛刻程度可以快速测试LOHCs的长效稳定性,例如Modisha等[117]通过提升Hn-DBT的脱氢温度测试了DBT的稳定性并分析了副产物,结果表明DBT具有较高的稳定性。总的来说,在数个乃至数十个周期内,NEC、DBT等LOHCs都具有较高的储释氢稳定性,但面向工业应用,尤其是在燃料电池车等运输工具中的应用,LOHCs需要在更长周期、更多循环中使用,其稳定性仍需相关实验数据确证。
Wang等[118]比较了N-乙基咔唑和高压储氢方式的能量利用效率,在该工作的设定条件(综合储存和运输)下,LOHCs材料(NEC)的能量利用效率低于高压储氢方式,只有在LOHCs材料加氢过程中释放的热量可以被利用的前提下,LOHCs的效率才与高压储氢方式持平。但是,Yang等[119]认为该工作过多地考虑了NEC催化脱氢后的循环衰变,从而低估了NEC的能量利用效率;同时,对高压储氢方式又没有考虑氢气压缩预冷和电机效率等因素,从而高估了高压储氢的效率。经核算,考虑上述因素后,35 MPa气罐、70 MPa气罐、NEC的能量利用效率分别约为88.3%、86%、88.7%,三者在整体上具有可比性。
在另一项研究中,Niermann等[16]对比了在特定条件下,不同LOHCs材料和高压储氢方式的技术水平与经济性。该研究假设了一种储运和使用氢气的流程框架:氢气从基于光伏系统的廉价发电地点(如中东和北非地区)经电解水制备,然后运至消费地点(如德国)被氢燃料电池利用。技术分析的结果显示,在题设条件下,LOHCs的工作效率主要受纯化氢气(尤其对于甲醇和甲酸体系,但其脱氢热较低)和脱氢加热的影响,N-乙基咔唑和二苄基甲苯体系的产物氢气无须纯化,且二者的储存、运输和整体链效率差别不大,但二者的储氢效率和整体链效率与压缩氢气相比都略有逊色。若认为燃料电池的废热可以抵消脱氢加热,则N-乙基咔唑和二苄基甲苯的效率可以进一步提升,整体链效率甚至超过了压缩氢气的效率。
从经济分析的角度,Niermann等[16]考虑安装、仪器仪表、管道、电气系统、建筑设施、工程建设、电价、LOHCs材料和催化剂的投资与运维等多种成本因素,重点计算氢化、运输和脱氢过程的成本。结果表明,即使考虑较高的原料成本(但由于LOHCs材料储氢可以循环利用,这一成本不应过高地考虑),包括N-乙基咔唑和二苄基甲苯在内的多种LOHCs材料都优于高压储氢方式。总的来说,排除原料价格的影响,二苄基甲苯和N-乙基咔唑在效率和经济性上都有较大的优势,这与之前关于这些材料性质的讨论相符。需要指出的是,尽管该工作讨论了N-乙基咔唑、二苄基甲苯、甲醇、甲酸等7种LOHCs和压缩氢气的效率,但作者并没有明确氢气的使用是否“车载(on-board)”,在文献中氢气仅作为能量的当量,故而未从可行性的角度加以分析。前已述及,从目前的技术来看,仅有N-乙基咔唑等杂环LOHCs材料具备车载用氢的可能性。
从上述讨论可以看出,面向应用的LOHCs研究一定要建立在具体使用场景的框架内,尤其是在分析LOHCs的经济性时。Teichmann等[120]讨论了不同储运场景下LOHCs和高压储氢、液相储氢的成本,结合等效年金方法,综合考虑运营费、能源成本和其他成本(例如氢损耗等),讨论了海上运输、公路运输以及释氢过程中不同储氢方法的差异。结果表明,相比于高压储氢和液相储氢,LOHCs储氢的设施成本与之差别不大,而能源损耗和运输成本则较低,具有较大的应用潜力。
需要强调的是,相比于高压储氢和固态储氢方式,LOHCs材料的优势并不局限于较高的能量利用效率和更有优势的成本,而更体现在针对基础设施的适配性、社会认同度等方面。例如为70 MPa压缩气罐服务的加氢站需要最高约90 MPa的压力[119],并且社会大众对于车载高压氢气的接受能力也可能限制其推广。同时,仍需考虑LOHCs材料的氢能源动力车与电动车的性能比较。经对比,氢阳公司“氢扬号”氢燃料电池大巴的续航里程(400 km)已超过城市常用的电动大巴(通常为150~250 km),但仍不及传统柴油车(通常可达700 km)。另外,随着燃料燃烧,化石燃料车的载重逐渐降低,可在一定程度上降低能耗,而LOHCs等新能源车不具备这个优势。
4.3 LOHCs商业化的技术难点综上所述,LOHCs材料已经具备一定的应用优势。目前适合于直接在机动车上释氢的LOHCs材料仍以含氮杂环化合物(N-乙基咔唑、N-丙基咔唑、N-甲基吲哚等)为主。需要指出,N-乙基咔唑在室温下呈固态,不利于移动源应用。目前的解决思路分为3类:第一类是使用溶剂,使之成为溶液[54]。第二类是控制脱氢反应的程度,使Hn-NEC不完全脱氢,利用中间产物(如H4-NEC)较低的熔点使体系呈液态。但这两种思路显然会降低LOHCs的实际储氢容量,使得整体效率降低。第三种思路是使用多种N-杂环的混合物作为LOHCs,使其熔点降低。例如,N-乙基咔唑[40]、N-丙基咔唑和N-丁基咔唑[121]的加氢反应焓和其他物理化学性质非常类似,观察其三元混合物相图[122],通过调节合适的混合比例,该共熔体的熔点可实现大幅降低,当N-乙基咔唑、N-丙基咔唑、N-丁基咔唑的物质的量之比为32∶41∶27时,共熔体的熔点仅为12 ℃,可在室温下以液态形式用于储氢。
此外,脱氢反应较高的焓变使加氢过程放出的热量可能被浪费,而脱氢反应又需要大量的热量,从而降低了LOHCs材料载氢的能量利用效率。碳环类化合物的焓变比杂环类更高,需要更多的热量和更加苛刻的反应条件[123]。从工业应用来看,LOHCs的加氢场景较为集中,放出的热量回用难度不大,但脱氢场景(车内或其他民用场所)往往较为分散,所需热量往往需要靠脱氢反应产生的氢气提供,这也是限制其有效储氢密度的重要因素。
碳环类LOHCs的催化脱氢温度往往较高,通常高于300 ℃[124-126],脱氢过程释放的氢气有较大一部分要用于为脱氢反应供能,使其难以应用于车船用氢燃料电池。Usman等[127]测算的结果表明,将一辆1.2 L排量的Honda Jazz 1.2汽车改装成使用甲苯作为储氢介质的氢燃料车,若达到原汽油车的性能,燃料储存空间需324.8 L(该车油箱大小仅为42 L)。相比而言,N-杂环LOHCs的脱氢温度一般仅有200 ℃左右,具有应用潜力,但即使低至200 ℃,这些LOHCs材料脱氢的能耗仍然难以由燃料电池的废热提供。解决此问题的思路有两个,一是直接使用LOHCs材料作为燃料电池的燃料(即在负极原位脱氢),省去释氢环节,但有机分子通常不导电,且缺乏此类化合物直接应用于电极材料释氢氧化的研究,因此实现此过程存在技术上的难度。二是利用该分子的特性提供额外的能量,在一份Air Products and Chemicals公司的专利文件[128]中,申请人公布了一种自热脱氢技术,指出可利用LOHCs分子的可逆选择性氧化提供脱氢热,例如使N-羟乙基咔唑的羟乙基在Pt基催化剂的存在下选择性氧化成羧甲基,反应放热约364 kJ/mol,可用于提供脱氢反应所需的能量。在此设计中,Hn-LOHC分子先脱氢生成H0-LOHC,并释放H2,H0-LOHC再发生选择性氧化,放出的热量为脱氢装置加热,并释放出部分氧化的LOHC分子,最终这些分子在加氢时一并还原。利用LOHC分子侧链的特性为脱氢反应供能是一种非常巧妙的思路,但这需要对LOHC分子进行一定程度的改造,例如将侧链上的官能团加以活化,但活化后的官能团或许又会影响脱氢反应中的活性与选择性,此外,额外的选择性氧化装置也会给燃料电池车的机械结构设计带来额外的负担。
5 总结与展望综上所述,LOHCs材料储氢作为一种常温常压的高效储氢方式有着重要的应用前景,但仍因一些技术上的问题需进一步优化。目前投入研究的LOHCs分子很多,但仅有以N-乙基咔唑和二苄基甲苯为代表的少数分子实现了工业示范,在交通运输储氢领域展现出一定的工业潜力。这两种体系在不同的细分领域各有优势,分别可以更好地适应不同的场景,随着LOHCs储氢系统相关技术的发展,它们在储能和供能方面都有极大潜力。
总的来说,应用于交通运输的储氢技术的目的仍可细分为以储运为主和以直接供能为主。LOHCs材料具备较强的工业化应用前景,尤其是在交通运输层面,因其在常温下多为液相,且较为安全、环境友好,便于运输和长期储存,适宜作为氢气储存和远距离输送的媒介。但若要应用于氢燃料电池车,仍需在上述问题以及氢燃料电池本身上产生突破。
在以储存为目的的LOHCs体系设计中,LOHCs有利于方便地将化石能源和太阳能、风能等一次能源收集起来,并作为二次能源在给定的时间和空间内加以利用。这一领域的LOHCs体系设计应关注大宗LOHCs分子的成本、安全性、可重复性等特征,在这一条件下,以二苄基甲苯为代表的碳环化合物具有一定优势,其也可以作为分布储能(加氢站储氢)和智能电网建设(削峰填谷)的储备材料。
面对以供能,尤其是以为移动源供氢为目的的LOHCs场景,应关注LOHCs的储氢密度、脱氢温度、释氢速率等因素,在这一领域N-乙基咔唑及其同系物具有一定的优势,其大宗合成、储存和运输有重要意义。
结合本文内容,LOHCs储氢体系发展的方向包括:(1)改性和发展新型LOHCs分子,使其能量密度更高、反应焓更低,甚至具备侧链可逆氧化供能的能力;(2)合成催化性能更高、贵金属活性组分含量更低(或非贵金属基)的脱氢催化剂;(3)将LOHCs直接应用于燃料电池负极,经原位脱氢作为燃料;(4)LOHCs分子大宗生产与降本增效;(5)模块化的加氢、储运、脱氢工程设计和设施建设等。这些发展方向各自独立又相互联系,在实际开发过程中应综合考虑LOHCs材料的性质、催化剂和催化装置、大宗生产等因素。
| [1] |
吴朝玲, 李永涛, 李媛, 等. 氢气储存和输运[M]. 北京: 化学工业出版社, 2021. WU C L, LI Y T, LI Y, et al. Hydrogen storage and transportation[M]. Beijing: Chemical Industry Press, 2021. (in Chinese) |
| [2] |
SCHLAPBACH L, ZVTTEL A. Hydrogen-storage materials for mobile applications[J]. Nature, 2001, 414(6861): 353-358. DOI:10.1038/35104634 |
| [3] |
YOSHIDA T, KOJIMA K. Toyota MIRAI fuel cell vehicle and progress toward a future hydrogen society[J]. Electrochemical Society Interface, 2015, 24(2): 45-49. DOI:10.1149/2.F03152if |
| [4] |
毛宗强, 王昌建, 李权. 氢安全[M]. 北京: 化学工业出版社, 2020. MAO Z Q, WANG C J, LI Q. Hydrogen safety[M]. Beijing: Chemical Industry Press, 2020. (in Chinese) |
| [5] |
SHERIF S A, ZEYTINOGLU N, VEZIROGLU T N. Liquid hydrogen: potential, problems, and a proposed research program[J]. International Journal of Hydrogen Energy, 1997, 22(7): 683-688. DOI:10.1016/S0360-3199(96)00201-7 |
| [6] |
VAN MAL H H, BUSCHOW K H J, MIEDEMA A R. Hydrogen absorption in LaNi5 and related compounds: experimental observations and their explanation[J]. Journal of the Less Common Metals, 1974, 35(1): 65-76. DOI:10.1016/0022-5088(74)90146-5 |
| [7] |
LIU X D, FENG H W, TIAN X, et al. Effects of additions on AB5-type hydrogen storage alloy in MH-Ni battery application[J]. International Journal of Hydrogen Energy, 2009, 34(17): 7291-7295. DOI:10.1016/j.ijhydene.2009.06.071 |
| [8] |
SAKINTUNA B, LAMARI-DARKRIM F, HIRSCHER M. Metal hydride materials for solid hydrogen storage: a review[J]. International Journal of Hydrogen Energy, 2007, 32(9): 1121-1140. DOI:10.1016/j.ijhydene.2006.11.022 |
| [9] |
DILLON A C, JONES K M, BEKKEDAHL T A, et al. Storage of hydrogen in single-walled carbon nanotubes[J]. Nature, 1997, 386(6623): 377-379. DOI:10.1038/386377a0 |
| [10] |
ORIMO S I, NAKAMORI Y, ELISEO J R, et al. Complex hydrides for hydrogen storage[J]. Chemical Reviews, 2007, 107(10): 4111-4132. DOI:10.1021/cr0501846 |
| [11] |
ROSI N L, ECKERT J, EDDAOUDI M, et al. Hydrogen storage in microporous metal-organic frameworks[J]. Science, 2003, 300(5622): 1127-1129. DOI:10.1126/science.1083440 |
| [12] |
SUH M P, PARK H J, PRASAD T K, et al. Hydrogen storage in metal-organic frameworks[J]. Chemical Reviews, 2012, 112(2): 782-835. DOI:10.1021/cr200274s |
| [13] |
蔡颖, 许剑轶, 胡锋, 等. 储氢技术与材料[M]. 北京: 化学工业出版社, 2018. CAI Y, XU J Y, HU F, et al. Hydrogen storage technologies and materials[M]. Beijing: Chemical Industry Press, 2018. (in Chinese) |
| [14] |
TAUBE M, RIPPIN D W T, CRESSWELL D L, et al. A system of hydrogen-powered vehicles with liquid organic hydrides[J]. International Journal of Hydrogen Energy, 1983, 8(3): 213-225. DOI:10.1016/0360-3199(83)90067-8 |
| [15] |
宋鹏飞, 侯建国, 穆祥宇, 等. 液体有机氢载体储氢体系筛选及应用场景分析[J]. 天然气化工(C1化学与化工), 2021, 46(1): 1-5, 33. SONG P F, HOU J G, MU X Y, et al. Screening and application scenarios of liquid organic hydrogen carrier systems[J]. Natural Gas Chemical Industry (C1 Chemistry and Chemical Engineering), 2021, 46(1): 1-5, 33. (in Chinese) |
| [16] |
NIERMANN M, DRVNERT S, KALTSCHMITT M, et al. Liquid organic hydrogen carriers (LOHCs)-techno-economic analysis of LOHCs in a defined process chain[J]. Energy & Environmental Science, 2019, 12(1): 290-307. |
| [17] |
中华人民共和国科学技术部. 关于对"十四五"国家重点研发计划"氢能技术"等18个重点专项2021年度项目申报指南征求意见的通知[EB/OL]. [2021-03-03]. https://service.most.gov.cn/kjjh_tztg_all/20210201/4186.html. Ministry of Science and Technology of the People's Republic of China. Notice on soliciting opinions on the 2021 project application guidelines for 18 key special projects including the "14th five-year" national key research and development plan "hydrogen energy technology"[EB/OL]. [2021-03-03]. https://service.most.gov.cn/kjjh_tztg_all/20210201/4186.html. (in Chinese) |
| [18] |
Hydrogen and Fuel Cell Technologies Office. DOE technical targets for onboard hydrogen storage for light-duty vehicles[EB/OL]. [2021-01-17]. https://www.energy.gov/eere/fuelcells/doe-technical-targets-onboard-hydrogen-storage-light-duty-vehicles.
|
| [19] |
TEICHMANN D, ARLT W, WASSERSCHEID P, et al. A future energy supply based on liquid organic hydrogen carriers (LOHC)[J]. Energy & Environmental Science, 2011, 4(8): 2767-2773. |
| [20] |
NEDO. The world's first global hydrogen supply chain demonstration project[EB/OL]. [2021-01-17]. https://www.mitsui.com/jp/en/release/2017/1224164_10832.html.
|
| [21] |
HODOSHIMA S, TAKAIWA S, SHONO A, et al. Hydrogen storage by decalin/naphthalene pair and hydrogen supply to fuel cells by use of superheated liquid-film-type catalysis[J]. Applied Catalysis A: General, 2005, 283(1-2): 235-242. DOI:10.1016/j.apcata.2005.01.010 |
| [22] |
BRVCKNER N, OBESSER K, BÖSMANN A, et al. Evaluation of industrially applied heat-transfer fluids as liquid organic hydrogen carrier systems[J]. ChemSusChem, 2014, 7(1): 229-235. DOI:10.1002/cssc.201300426 |
| [23] |
Hydrogenious LOHC Technologies. Products[EB/OL]. [2021-01-17]. https://www.hydrogenious.net/index.php/en/products.
|
| [24] |
SOTOODEH F, HUBER B J M, SMITH K J. The effect of the N atom on the dehydrogenation of heterocycles used for hydrogen storage[J]. Applied Catalysis A: General, 2012, 419-420: 67-72. DOI:10.1016/j.apcata.2012.01.013 |
| [25] |
HIYOSHI N, RODE C V, SATO O, et al. Biphenyl hydrogenation over supported transition metal catalysts under supercritical carbon dioxide solvent[J]. Applied Catalysis A: General, 2005, 288(1-2): 43-47. DOI:10.1016/j.apcata.2005.04.021 |
| [26] |
JANG M, JO Y S, LEE W J, et al. A high-capacity, reversible liquid organic hydrogen carrier: H2-release properties and an application to a fuel cell[J]. ACS Sustainable Chemistry & Engineering, 2019, 7(1): 1185-1194. |
| [27] |
ZHU Q L, XU Q. Liquid organic and inorganic chemical hydrides for high-capacity hydrogen storage[J]. Energy & Environmental Science, 2015, 8(2): 478-512. |
| [28] |
TAN K C, YU Y, CHEN R, et al. Metallo-N-heterocycles—a new family of hydrogen storage material[J]. Energy Storage Materials, 2020, 26: 198-202. DOI:10.1016/j.ensm.2019.12.035 |
| [29] |
DONG Y, YANG M, YANG Z H, et al. Catalytic hydrogenation and dehydrogenation of N-ethylindole as a new heteroaromatic liquid organic hydrogen carrier[J]. International Journal of Hydrogen Energy, 2015, 40(34): 10918-10922. DOI:10.1016/j.ijhydene.2015.05.196 |
| [30] |
DONG Y, YANG M, LI L L, et al. Study on reversible hydrogen uptake and release of 1, 2-dimethylindole as a new liquid organic hydrogen carrier[J]. International Journal of Hydrogen Energy, 2019, 44(10): 4919-4929. DOI:10.1016/j.ijhydene.2019.01.015 |
| [31] |
YAMAGUCHI R, IKEDA C, TAKAHASHI Y, et al. Homogeneous catalytic system for reversible dehydrogenation-hydrogenation reactions of nitrogen heterocycles with reversible interconversion of catalytic species[J]. Journal of the American Chemical Society, 2009, 131(24): 8410-8412. DOI:10.1021/ja9022623 |
| [32] |
FORBERG D, SCHWOB T, ZAHEER M, et al. Single-catalyst high-weight% hydrogen storage in an N-heterocycle synthesized from lignin hydrogenolysis products and ammonia[J]. Nature Communications, 2016, 7(1): 13201. DOI:10.1038/ncomms13201 |
| [33] |
YU Y, HE T, WU A N, et al. Reversible hydrogen uptake/release over a sodium phenoxide-cyclohexanolate pair[J]. Angewandte Chemie International Edition, 2019, 58(10): 3102-3107. DOI:10.1002/anie.201810945 |
| [34] |
LI P Z, AIJAZ A, XU Q. Highly dispersed surfactant-free nickel nanoparticles and their remarkable catalytic activity in the hydrolysis of ammonia borane for hydrogen generation[J]. Angewandte Chemie International Edition, 2012, 51(27): 6753-6756. DOI:10.1002/anie.201202055 |
| [35] |
LIN L L, ZHOU W, GAO R, et al. Low-temperature hydrogen production from water and methanol using Pt/α-MoC catalysts[J]. Nature, 2017, 544(7648): 80-83. DOI:10.1038/nature21672 |
| [36] |
NIELSEN M, ALBERICO E, BAUMANN W, et al. Low-temperature aqueous-phase methanol dehydrogenation to hydrogen and carbon dioxide[J]. Nature, 2013, 495(7439): 85-89. DOI:10.1038/nature11891 |
| [37] |
HU P, FOGLER E, DISKIN-POSNER Y, et al. A novel liquid organic hydrogen carrier system based on catalytic peptide formation and hydrogenation[J]. Nature Communications, 2015, 6(1): 6859. DOI:10.1038/ncomms7859 |
| [38] |
RAO P C, YOON M. Potential liquid-organic hydrogen carrier (LOHC) systems: a review on recent progress[J]. Energies, 2020, 13(22): 6040. DOI:10.3390/en13226040 |
| [39] |
AAKKO-SAKSA P T, COOK C, KIVIAHO J, et al. Liquid organic hydrogen carriers for transportation and storing of renewable energy—review and discussion[J]. Journal of Power Sources, 2018, 396: 803-823. DOI:10.1016/j.jpowsour.2018.04.011 |
| [40] |
NIERMANN M, BECKENDORFF A, KALTSCHMITT M, et al. Liquid organic hydrogen carrier (LOHC)—assessment based on chemical and economic properties[J]. International Journal of Hydrogen Energy, 2019, 44(13): 6631-6654. DOI:10.1016/j.ijhydene.2019.01.199 |
| [41] |
CHEN Z W, YANG M, ZHU T, et al. 7-ethylindole: a new efficient liquid organic hydrogen carrier with fast kinetics[J]. International Journal of Hydrogen Energy, 2018, 43(28): 12688-12696. DOI:10.1016/j.ijhydene.2018.03.088 |
| [42] |
VEREVKIN S P, PIMERZIN A A, SUN L X. Liquid organic hydrogen carriers: hydrogen storage by di-phenyl ether derivatives: an experimental and theoretical study[J]. The Journal of Chemical Thermodynamics, 2020, 144: 106057. DOI:10.1016/j.jct.2020.106057 |
| [43] |
EBLAGON K M, TSANG S C E. Structure-reactivity relationship in catalytic hydrogenation of heterocyclic compounds over ruthenium black; Part B: effect of carbon substitution by heteroatom[J]. Applied Catalysis B: Environmental, 2015, 163: 599-610. DOI:10.1016/j.apcatb.2014.08.040 |
| [44] |
HE T, PEI Q J, CHEN P. Liquid organic hydrogen carriers[J]. Journal of Energy Chemistry, 2015, 24(5): 587-594. DOI:10.1016/j.jechem.2015.08.007 |
| [45] |
GIANOTTI E, TAILLADES-JACQUIN M, ROZIÈRE J, et al. High-purity hydrogen generation via dehydrogenation of organic carriers: a review on the catalytic process[J]. ACS Catalysis, 2018, 8(5): 4660-4680. DOI:10.1021/acscatal.7b04278 |
| [46] |
YANG M, DONG Y, FEI S X, et al. A comparative study of catalytic dehydrogenation of perhydro-N-ethylcarbazole over noble metal catalysts[J]. International Journal of Hydrogen Energy, 2014, 39(33): 18976-18983. DOI:10.1016/j.ijhydene.2014.09.123 |
| [47] |
WANG B, CHANG T Y, JIANG Z, et al. Catalytic dehydrogenation study of dodecahydro-N-ethylcarbazole by noble metal supported on reduced graphene oxide[J]. International Journal of Hydrogen Energy, 2018, 43(15): 7317-7325. DOI:10.1016/j.ijhydene.2018.02.156 |
| [48] |
SOTOODEH F, SMITH K J. Analysis of H2 release from organic polycyclics over Pd catalysts using DFT[J]. The Journal of Physical Chemistry C, 2013, 117(1): 194-204. DOI:10.1021/jp307325s |
| [49] |
DONG Y, YANG M, ZHU T, et al. Fast dehydrogenation kinetics of perhydro-N-propylcarbazole over a supported Pd catalyst[J]. ACS Applied Energy Materials, 2018, 1(8): 4285-4292. DOI:10.1021/acsaem.8b00914 |
| [50] |
GLEICHWEIT C, AMENDE M, BAUER U, et al. Alkyl chain length-dependent surface reaction of dodecahydro-N-alkylcarbazoles on Pt model catalysts[J]. The Journal of Chemical Physics, 2014, 140(20): 204711. DOI:10.1063/1.4875921 |
| [51] |
YANG M, DONG Y, FEI S X, et al. Hydrogenation of N-propylcarbazole over supported ruthenium as a new prototype of liquid organic hydrogen carriers (LOHC)[J]. RSC Advances, 2013, 3(47): 24877-24881. DOI:10.1039/c3ra44760j |
| [52] |
SOBOTA M, NIKIFORIDIS I, AMENDE M, et al. Dehydrogenation of dodecahydro-N-ethylcarbazole on Pd/Al2O3 model catalysts[J]. Chemistry—A European Journal, 2011, 17(41): 11542-11552. DOI:10.1002/chem.201101311 |
| [53] |
GLEICHWEIT C, AMENDE M, SCHERNICH S, et al. Dehydrogenation of dodecahydro-N-ethylcarbazole on Pt (111)[J]. ChemSusChem, 2013, 6(6): 974-977. DOI:10.1002/cssc.201300263 |
| [54] |
SOTOODEH F, SMITH K J. Structure sensitivity of dodecahydro-N-ethylcarbazole dehydrogenation over Pd catalysts[J]. Journal of Catalysis, 2011, 279(1): 36-47. DOI:10.1016/j.jcat.2010.12.022 |
| [55] |
SOTOODEH F, HUBER B J M, SMITH K J. Dehydrogenation kinetics and catalysis of organic heteroaromatics for hydrogen storage[J]. International Journal of Hydrogen Energy, 2012, 37(3): 2715-2722. DOI:10.1016/j.ijhydene.2011.03.055 |
| [56] |
AMENDE M, GLEICHWEIT C, SCHERNICH S, et al. Size and structure effects controlling the stability of the liquid organic hydrogen carrier dodecahydro-N-ethylcarbazole during dehydrogenation over Pt model catalysts[J]. The Journal of Physical Chemistry Letters, 2014, 5(8): 1498-1504. DOI:10.1021/jz500157r |
| [57] |
WANG B, CHEN Y T, CHANG T Y, et al. Facet-dependent catalytic activities of Pd/rGO: exploring dehydrogenation mechanism of dodecahydro-N-ethylcarbazole[J]. Applied Catalysis B: Environmental, 2020, 266: 118658. DOI:10.1016/j.apcatb.2020.118658 |
| [58] |
SOTOODEH F, ZHAO L, SMITH K J. Kinetics of H2 recovery from dodecahydro-N-ethylcarbazole over a supported Pd catalyst[J]. Applied Catalysis A: General, 2009, 362(1): 155-162. |
| [59] |
DONG Y, YANG M, MEI P, et al. Dehydrogenation kinetics study of perhydro-N-ethylcarbazole over a supported Pd catalyst for hydrogen storage application[J]. International Journal of Hydrogen Energy, 2016, 41(20): 8498-8505. DOI:10.1016/j.ijhydene.2016.03.157 |
| [60] |
MOLINER M, GABAY J E, KLIEWER C E, et al. Reversible transformation of Pt nanoparticles into single atoms inside high-silica chabazite zeolite[J]. Journal of the American Chemical Society, 2016, 138(48): 15743-15750. DOI:10.1021/jacs.6b10169 |
| [61] |
LIU A N, LIU X, LIU L C, et al. Getting insights into the temperature-specific active sites on platinum nanoparticles for CO oxidation: a combined in situ spectroscopic and ab initio density functional theory study[J]. ACS Catalysis, 2019, 9(9): 7759-7768. DOI:10.1021/acscatal.9b02552 |
| [62] |
LIU A N, LIU L C, CAO Y, et al. Controlling dynamic structural transformation of atomically dispersed CuOx species and influence on their catalytic performances[J]. ACS Catalysis, 2019, 9(11): 9840-9851. DOI:10.1021/acscatal.9b02773 |
| [63] |
JIANG Z, GONG X, GUO S Y, et al. Engineering PdCu and PdNi bimetallic catalysts with adjustable alloying degree for the dehydrogenation reaction of dodecahydro-N-ethylcarbazole[J]. International Journal of Hydrogen Energy, 2021, 46(2): 2376-2389. DOI:10.1016/j.ijhydene.2020.10.123 |
| [64] |
CHEN X D, LI G, GAO M, et al. Wet-impregnated bimetallic Pd-Ni catalysts with enhanced activity for dehydrogenation of perhydro-N-propylcarbazole[J]. International Journal of Hydrogen Energy, 2020, 45(56): 32168-32178. DOI:10.1016/j.ijhydene.2020.08.162 |
| [65] |
WANG B, CHANG T Y, JIANG Z, et al. Component controlled synthesis of bimetallic PdCu nanoparticles supported on reduced graphene oxide for dehydrogenation of dodecahydro-N-ethylcarbazole[J]. Applied Catalysis B: Environmental, 2019, 251: 261-272. DOI:10.1016/j.apcatb.2019.03.071 |
| [66] |
WANG B, CHANG T Y, GONG X, et al. One-pot synthesis of Au/Pd core/shell nanoparticles supported on reduced graphene oxide with enhanced dehydrogenation performance for dodecahydro-N-ethylcarbazole[J]. ACS Sustainable Chemistry & Engineering, 2019, 7(1): 1760-1768. |
| [67] |
JIANG Z, GUO S Y, FANG T. Enhancing the catalytic activity and selectivity of PdAu/SiO2 bimetallic catalysts for dodecahydro-N-ethylcarbazole dehydrogenation by controlling the particle size and dispersion[J]. ACS Applied Energy Materials, 2019, 2(10): 7233-7243. DOI:10.1021/acsaem.9b01202 |
| [68] |
KUSTOV L M, TARASOV A L, KIRICHENKO O A. Microwave-activated dehydrogenation of perhydro-N-ethylcarbazol over bimetallic Pd-M/TiO2 catalysts as the second stage of hydrogen storage in liquid substrates[J]. International Journal of Hydrogen Energy, 2017, 42(43): 26723-26729. DOI:10.1016/j.ijhydene.2017.09.009 |
| [69] |
GONG X, JIANG Z, FANG T. Enhancing selectivity and reducing cost for dehydrogenation of dodecahydro-N-ethylcarbazole by supporting platinum on titanium dioxide[J]. International Journal of Hydrogen Energy, 2020, 45(11): 6838-6847. DOI:10.1016/j.ijhydene.2019.12.203 |
| [70] |
JIANG Z, GONG X, WANG B, et al. A experimental study on the dehydrogenation performance of dodecahydro-N-ethylcarbazole on M/TiO2 catalysts[J]. International Journal of Hydrogen Energy, 2019, 44(5): 2951-2959. DOI:10.1016/j.ijhydene.2018.11.236 |
| [71] |
JIANG Z, PAN Q, XU J, et al. Current situation and prospect of hydrogen storage technology with new organic liquid[J]. International Journal of Hydrogen Energy, 2014, 39(30): 17442-17451. DOI:10.1016/j.ijhydene.2014.01.199 |
| [72] |
DING C H, ZHU T, WANG F Y, et al. High active Pd@mil-101 catalyst for dehydrogenation of liquid organic hydrogen carrier[J]. International Journal of Hydrogen Energy, 2020, 45(32): 16144-16152. DOI:10.1016/j.ijhydene.2020.04.081 |
| [73] |
ZHU M Y, XU L X, DU L, et al. Palladium supported on carbon nanotubes as a high-performance catalyst for the dehydrogenation of dodecahydro-N-ethylcarbazole[J]. Catalysts, 2018, 8(12): 638. DOI:10.3390/catal8120638 |
| [74] |
ALHUMAIDAN F, TSAKIRIS D, CRESSWELL D, et al. Hydrogen storage in liquid organic hydride: selectivity of MCH dehydrogenation over monometallic and bimetallic Pt catalysts[J]. International Journal of Hydrogen Energy, 2013, 38(32): 14010-14026. DOI:10.1016/j.ijhydene.2013.08.067 |
| [75] |
MVLLER K, STARK K, EMEL'YANENKO V N, et al. Liquid organic hydrogen carriers: thermophysical and thermochemical studies of benzyl- and dibenzyl-toluene derivatives[J]. Industrial & Engineering Chemistry Research, 2015, 54(32): 7967-7976. |
| [76] |
JORSCHICK H, GEIΒELBRECHT M, EΒL M, et al. Benzyltoluene/dibenzyltoluene-based mixtures as suitable liquid organic hydrogen carrier systems for low temperature applications[J]. International Journal of Hydrogen Energy, 2020, 45(29): 14897-14906. DOI:10.1016/j.ijhydene.2020.03.210 |
| [77] |
MVLLER K, ASLAM R, FISCHER A, et al. Experimental assessment of the degree of hydrogen loading for the dibenzyl toluene based LOHC system[J]. International Journal of Hydrogen Energy, 2016, 41(47): 22097-22103. DOI:10.1016/j.ijhydene.2016.09.196 |
| [78] |
MODISHA P, GQOGQA P, GARIDZIRAI R, et al. Evaluation of catalyst activity for release of hydrogen from liquid organic hydrogen carriers[J]. International Journal of Hydrogen Energy, 2019, 44(39): 21926-21935. DOI:10.1016/j.ijhydene.2019.06.212 |
| [79] |
USMAN M R, CRESSWELL D L, GARFORTH A A. By-products formation in the dehydrogenation of methylcyclohexane[J]. Petroleum Science and Technology, 2011, 29(21): 2247-2257. DOI:10.1080/10916466.2011.584103 |
| [80] |
OKADA Y, IMAGAWA K, YASUIC M. Development of novel dehydrogenation catalyst for hydrogen carrier system[C]//The 8th Tokyo Conference on Advanced Catalytic Science and Technology (TOCAT 8). Yokohama, 2018.
|
| [81] |
AUER F, BLAUMEISER D, BAUER T, et al. Boosting the activity of hydrogen release from liquid organic hydrogen carrier systems by sulfur-additives to Pt on alumina catalysts[J]. Catalysis Science & Technology, 2019, 9(13): 3537-3547. |
| [82] |
PATIL S P, PANDE J V, BINIWALE R B. Non-noble Ni-Cu/ACC bimetallic catalyst for dehydrogenation of liquid organic hydrides for hydrogen storage[J]. International Journal of Hydrogen Energy, 2013, 38(35): 15233-15241. DOI:10.1016/j.ijhydene.2013.09.115 |
| [83] |
GARIDZIRAI R, MODISHA P, SHURO I, et al. The effect of Mg and Zn dopants on Pt/Al2O3 for the dehydrogenation of perhydrodibenzyltoluene[J]. Catalysts, 2021, 11(4): 490. DOI:10.3390/catal11040490 |
| [84] |
CHEN X M, GIERLICH C H, SCHÖTZ S, et al. Hydrogen production based on liquid organic hydrogen carriers through sulfur doped platinum catalysts supported on TiO2[J]. ACS Sustainable Chemistry & Engineering, 2021, 9(5): 6561-6573. |
| [85] |
LEE S, LEE J, KIM T, et al. Pt/CeO2 catalyst synthesized by combustion method for dehydrogenation of perhydro-dibenzyltoluene as liquid organic hydrogen carrier: effect of pore size and metal dispersion[J]. International Journal of Hydrogen Energy, 2021, 46(7): 5520-5529. DOI:10.1016/j.ijhydene.2020.11.038 |
| [86] |
AAKKO-SAKSA P T, VEHKAMÄKI M, KEMELL M, et al. Hydrogen release from liquid organic hydrogen carriers catalysed by platinum on rutile-anatase structured titania[J]. Chemical Communications, 2020, 56(11): 1657-1660. DOI:10.1039/C9CC09715E |
| [87] |
SHI L B, QI S T, QU J F, et al. Integration of hydrogenation and dehydrogenation based on dibenzyltoluene as liquid organic hydrogen energy carrier[J]. International Journal of Hydrogen Energy, 2019, 44(11): 5345-5354. DOI:10.1016/j.ijhydene.2018.09.083 |
| [88] |
WAN C, AN Y, XU G H, et al. Study of catalytic hydrogenation of N-ethylcarbazole over ruthenium catalyst[J]. International Journal of Hydrogen Energy, 2012, 37(17): 13092-13096. DOI:10.1016/j.ijhydene.2012.04.123 |
| [89] |
EBLAGON K M, TAM K, YU K M K, et al. Comparative study of catalytic hydrogenation of 9-ethylcarbazole for hydrogen storage over noble metal surfaces[J]. The Journal of Physical Chemistry C, 2012, 116(13): 7421-7429. DOI:10.1021/jp212249g |
| [90] |
EBLAGON K M, RENTSCH D, FRIEDRICHS O, et al. Hydrogenation of 9-ethylcarbazole as a prototype of a liquid hydrogen carrier[J]. International Journal of Hydrogen Energy, 2010, 35(20): 11609-11621. DOI:10.1016/j.ijhydene.2010.03.068 |
| [91] |
YE X F, AN Y, XU G H. Kinetics of 9-ethylcarbazole hydrogenation over Raney-Ni catalyst for hydrogen storage[J]. Journal of Alloys and Compounds, 2011, 509(1): 152-156. DOI:10.1016/j.jallcom.2010.09.012 |
| [92] |
WAN C, AN Y, CHEN F Q, et al. Kinetics of N-ethylcarbazole hydrogenation over a supported Ru catalyst for hydrogen storage[J]. International Journal of Hydrogen Energy, 2013, 38(17): 7065-7069. DOI:10.1016/j.ijhydene.2013.04.022 |
| [93] |
EBLAGON K M, TAM K, TSANG S C E. Comparison of catalytic performance of supported ruthenium and rhodium for hydrogenation of 9-ethylcarbazole for hydrogen storage applications[J]. Energy & Environmental Science, 2012, 5(9): 8621-8630. |
| [94] |
FEI S X, HAN B, LI L L, et al. A study on the catalytic hydrogenation of N-ethylcarbazole on the mesoporous Pd/MoO3 catalyst[J]. International Journal of Hydrogen Energy, 2017, 42(41): 25942-25950. DOI:10.1016/j.ijhydene.2017.08.204 |
| [95] |
LI P J, DONG Y, DING Y H, et al. Effect of hydrogen spillover on the surface of tungsten oxide on hydrogenation of cyclohexene and N-propylcarbazole[J]. International Journal of Hydrogen Energy, 2021, 46(5): 3945-3953. DOI:10.1016/j.ijhydene.2020.10.230 |
| [96] |
YU H E, YANG X, WU Y, et al. Bimetallic Ru-Ni/TiO2 catalysts for hydrogenation of N-ethylcarbazole: role of TiO2 crystal structure[J]. Journal of Energy Chemistry, 2020, 40: 188-195. DOI:10.1016/j.jechem.2019.04.009 |
| [97] |
WU Y, YU H E, GUO Y R, et al. A rare earth hydride supported ruthenium catalyst for the hydrogenation of N-heterocycles: boosting the activity via a new hydrogen transfer path and controlling the stereoselectivity[J]. Chemical Science, 2019, 10(45): 10459-10465. DOI:10.1039/C9SC04365A |
| [98] |
EBLAGON K M, TAM K, YU K M K, et al. Study of catalytic sites on ruthenium for hydrogenation of N-ethylcarbazole: implications of hydrogen storage via reversible catalytic hydrogenation[J]. The Journal of Physical Chemistry C, 2010, 114(21): 9720-9730. DOI:10.1021/jp908640k |
| [99] |
ALI A, KUMAR G U, LEE H J. Investigation of hydrogenation of dibenzyltoluene as liquid organic hydrogen carrier[J]. Materials Today: Proceedings, 2021, 45(5): 1123-1127. |
| [100] |
DO G, PREUSTER P, ASLAM R, et al. Hydrogenation of the liquid organic hydrogen carrier compound dibenzyltoluene-reaction pathway determination by 1H NMR spectroscopy[J]. Reaction Chemistry & Engineering, 2016, 1(3): 313-320. |
| [101] |
JORSCHICK H, PREUSTER P, BÖSMANN A, et al. Hydrogenation of aromatic and heteroaromatic compounds—a key process for future logistics of green hydrogen using liquid organic hydrogen carrier systems[J]. Sustainable Energy & Fuels, 2021, 5(5): 1311-1346. |
| [102] |
LEINWEBER A, MVLLER K. Hydrogenation of the liquid organic hydrogen carrier compound monobenzyl toluene: reaction pathway and kinetic effects[J]. Energy Technology, 2018, 6(3): 513-520. DOI:10.1002/ente.201700376 |
| [103] |
ZHU T, YANG M, CHEN X D, et al. A highly active bifunctional Ru-Pd catalyst for hydrogenation and dehydrogenation of liquid organic hydrogen carriers[J]. Journal of Catalysis, 2019, 378: 382-391. DOI:10.1016/j.jcat.2019.08.032 |
| [104] |
XUE W J, LIU H X, MAO B H, et al. Reversible hydrogenation and dehydrogenation of N-ethylcarbazole over bimetallic Pd-Rh catalyst for hydrogen storage[J]. Chemical Engineering Journal, 2020, 421(36): 127781. |
| [105] |
Institute for Micro Process Engineering. Kopernikus project: power-to-X research cluster B1 hydrogen carriers[EB/OL]. [2021-03-04]. https://www.imvt.kit.edu/english/1282_993.php.
|
| [106] |
MODISHA P M, OUMA C N M, GARIDZIRAI R, et al. The prospect of hydrogen storage using liquid organic hydrogen carriers[J]. Energy & Fuels, 2019, 33(4): 2778-2796. |
| [107] |
SHUKLA A, KARMAKAR S, BINIWALE R B. Hydrogen delivery through liquid organic hydrides: considerations for a potential technology[J]. International Journal of Hydrogen Energy, 2012, 37(4): 3719-3726. DOI:10.1016/j.ijhydene.2011.04.107 |
| [108] |
FIKRT A, BREHMER R, MILELLA V-O, et al. Dynamic power supply by hydrogen bound to a liquid organic hydrogen carrier[J]. Applied Energy, 2017, 194: 1-8. DOI:10.1016/j.apenergy.2017.02.070 |
| [109] |
BULGARIN A, JORSCHICK H, PREUSTER P, et al. Purity of hydrogen released from the liquid organic hydrogen carrier compound perhydro dibenzyltoluene by catalytic dehydrogenation[J]. International Journal of Hydrogen Energy, 2020, 45(1): 712-720. DOI:10.1016/j.ijhydene.2019.10.067 |
| [110] |
H2 Industries. LOHC technology turns hydrogen into a safe power storage technology[EB/OL]. [2021-01-17]. https://h2-industries.com/zh-hans/technology/.
|
| [111] |
武汉氢阳能源有限公司. 技术成果[EB/OL]. [2021-01-17]. http://www.hynertech.com/col.jsp?id=153. Hynertech Co., Ltd. . Technical achievements[EB/OL]. [2021-01-17]. http://www.hynertech.com/col.jsp?id=153. (in Chinese) |
| [112] |
CHENG H S, WU J P, DONG Y, et al. Liquid hydrogen storage system: US 2018/065849 A1[P]. 2018-03-08.
|
| [113] |
ALI A, KUMAR G U, LEE H J. Catalytic hydrogenation and dehydrogenation performance of 9-ethylcarbazole as a liquid organic hydrogen carrier[J]. Journal of Mechanical Science and Technology, 2019, 33(11): 5561-5569. DOI:10.1007/s12206-019-1049-8 |
| [114] |
叶旭峰, 安越, 许筠芸, 等. 乙基咔唑液相循环储放氢性能研究[J]. 化学工程, 2011, 39(6): 29-31, 58. YE X F, AN Y, XU Y Y, et al. Properties of cyclic sorption-desorption of hydrogen with liquid phase N-ethylcarbazole[J]. Chemical Engineering, 2011, 39(6): 29-31, 58. (in Chinese) DOI:10.3969/j.issn.1005-9954.2011.06.008 |
| [115] |
JORSCHICK H, PREUSTER P, DVRR S, et al. Hydrogen storage using a hot pressure swing reactor[J]. Energy & Environmental Science, 2017, 10(7): 1652-1659. |
| [116] |
JORSCHICK H, DVRR S, PREUSTER P, et al. Operational stability of a LOHC-based hot pressure swing reactor for hydrogen storage[J]. Energy Technology, 2019, 7(1): 146-152. DOI:10.1002/ente.201800499 |
| [117] |
MODISHA P, BESSARABOV D. Stress tolerance assessment of dibenzyltoluene-based liquid organic hydrogen carriers[J]. Sustainable Energy & Fuels, 2020, 4(9): 4662-4670. |
| [118] |
WANG H W, ZHOU X, OUYANG M G. Efficiency analysis of novel liquid organic hydrogen carrier technology and comparison with high pressure storage pathway[J]. International Journal of Hydrogen Energy, 2016, 41(40): 18062-18071. DOI:10.1016/j.ijhydene.2016.08.003 |
| [119] |
YANG M, SUN Y L, CHENG H S. Comments on "efficiency analysis of novel liquid organic hydrogen carrier technology and comparison with high pressure storage pathway"[Int. J. Hydrogen Energy 41 (2016) 18062-18071][J]. International Journal of Hydrogen Energy, 2017, 42(47): 28647-28648. DOI:10.1016/j.ijhydene.2017.09.034 |
| [120] |
TEICHMANN D, ARLT W, WASSERSCHEID P. Liquid organic hydrogen carriers as an efficient vector for the transport and storage of renewable energy[J]. International Journal of Hydrogen Energy, 2012, 37(23): 18118-18132. DOI:10.1016/j.ijhydene.2012.08.066 |
| [121] |
EMEL'YANENKO V N, VARFOLOMEEV M A, VEREVKIN S P, et al. Hydrogen storage: thermochemical studies of N-alkylcarbazoles and their derivatives as a potential liquid organic hydrogen carriers[J]. The Journal of Physical Chemistry C, 2015, 119(47): 26381-26389. DOI:10.1021/acs.jpcc.5b10392 |
| [122] |
STARK K, KEIL P, SCHUG S, et al. Melting points of potential liquid organic hydrogen carrier systems consisting of N-alkylcarbazoles[J]. Journal of Chemical & Engineering Data, 2016, 61(4): 1441-1448. |
| [123] |
SCHILDHAUER T, NEWSON E, MVLLER S. The equilibrium constant for the methylcyclohexane-toluene system[J]. Journal of Catalysis, 2001, 198(2): 355-358. DOI:10.1006/jcat.2000.3133 |
| [124] |
USMAN M R. The catalytic dehydrogenation of methylcyclohexane over monometallic catalysts for on-board hydrogen storage, production, and utilization[J]. Energy Sources, Part A: Recovery, Utilization, and Environmental Effects, 2011, 33(24): 2231-2238. DOI:10.1080/15567036.2011.565307 |
| [125] |
KOSAKA M, HIGO T, OGO S, et al. Low-temperature selective dehydrogenation of methylcyclohexane by surface protonics over Pt/anatase-TiO2 catalyst[J]. International Journal of Hydrogen Energy, 2020, 45(1): 738-743. DOI:10.1016/j.ijhydene.2019.10.133 |
| [126] |
WIJAYANTA A T, ODA T, PURNOMO C W, et al. Liquid hydrogen, methylcyclohexane, and ammonia as potential hydrogen storage: comparison review[J]. International Journal of Hydrogen Energy, 2019, 44(29): 15026-15044. DOI:10.1016/j.ijhydene.2019.04.112 |
| [127] |
USMAN M R, CRESSWELL D L. Options for on-board use of hydrogen based on the methylcyclohexane-toluene-hydrogen system[J]. International Journal of Green Energy, 2013, 10(2): 177-189. DOI:10.1080/15435075.2011.647168 |
| [128] |
PEZ G P, COOPER A C, SCOTT A R. Autothermal hydrogen storage and delivery systems: WO 2009/005872 A2[P]. 2009-01-08.
|