2. 海南大学 海南省特种玻璃重点实验室, 海口 570228;
3. 海南大学 南海海洋资源利用国家重点实验室, 海口 570228
2. Special Glass Key Lab of Hainan Province, Hainan University, Haikou 570228, China;
3. State Key Laboratory of Marine Resource Utilization in South China Sea, Hainan University, Haikou 570228, China
氮氧化物(NOx)是当前大气中的主要污染物之一,会带来大量环境问题,例如酸雨、PM2.5和光化学污染等[1]。为了减少氮氧化物带来的危害,人们研发了一系列的氮氧化物净化处理技术,例如选择性催化还原法(SCR)、非选择性催化还原法(NSCR)和等离子体技术等。其中,氨选择性催化还原法(NH3-SCR)由于成本低廉且净化效率高而被广泛应用。该方法主要通过标准SCR反应(式(1))和快速SCR反应(式(2))实现氮氧化物的无害化处理[2]。
| $ {4{\rm{N}}{{\rm{H}}_3} + 4{\rm{NO}} + {{\rm{O}}_2} = 4{{\rm{N}}_2} + 6{{\rm{H}}_2}{\rm{O}}} $ | (1) |
| $ {2{\rm{N}}{{\rm{H}}_3} + {\rm{NO}} + {\rm{N}}{{\rm{O}}_2} = 2{{\rm{N}}_2} + 3{{\rm{H}}_2}{\rm{O}}} $ | (2) |
在NH3-SCR技术中最关键的因素是催化剂,目前,商用V2O5-WO3(MoO3)/TiO2催化剂是在固定源(火力发电厂、燃煤锅炉等)中使用最广泛的SCR催化剂,该催化剂在300~400 ℃的温度区间表现出优异的氮氧化物去除效率,并且催化剂本身的抗压强度和耐磨性极佳。然而,V2O5-WO3(MoO3)/TiO2催化剂仍然有一些不可避免的缺陷,例如在低温范围内催化剂的活性很低,抗毒性差,并且催化剂中的V2O5易挥发、产生生物毒性。此外,该催化剂在高温下会产生大量N2O,降低了对N2的选择性[3]。因此,近年来许多研究致力于开发有效的非钒基催化剂[4]。在所有的非钒基催化剂中铈基催化剂被认为是最有潜力的替代品。原因是CeO2具有灵活多变的价态构成、表面有丰富的氧空位并且与NH3/NO有强相互作用,故作为助剂、载体或催化活性组分而被广泛应用于NH3-SCR催化剂的研究中[5-6]。但是,由于纯CeO2的表面上缺少SCR反应所需的酸性位点,其通常会表现出较低的催化活性。此外,在高温下,纯CeO2的表面会发生NH3的非选择性氧化,使催化剂对N2的选择性降低。研究表明,为铈基催化剂提供合适的载体可以尽可能地优化Ce在通道上的分散[7]。TiO2由于比表面积大,能以孔体积为催化活性中心,并且成本低廉、环境友好,因而常被用作催化剂的载体[8]。
目前,随着国家环境保护标准的不断提高,生物质燃料等可再生能源的使用已越来越广泛,但是生物质燃料的燃烧会产生高含量的K2O。无论是钒基还是非钒基的脱硝催化剂都会在这一过程中受到K2O的毒害作用而失活。因此,研究SCR催化剂抗碱中毒机制具有重要意义。根据Kamata等[9]的研究,V2O5-WO3/TiO2的催化活性与碱金属的沉积量有关,随着K2O添加量逐渐提高,V2O5-WO3/TiO2催化剂对NO的催化还原能力会随之降低。当沉积了质量分数约为1%的K2O后,催化剂几乎完全失活。Peng等[10]研究了碱金属对CeO2-WO3催化剂的影响,指出碱金属主要影响催化剂表面酸位的数量而不是酸强度,碱金属会抑制NOx与NH3之间的反应。Zhang等[11]将Mn-Ce/TiO2催化剂表面浸渍了少量钾盐,以模拟烟道气中的钾中毒,发现K+的引入严重影响了催化剂的低温活性,这是因为K+会以离子交换的形式占据布朗斯特酸表面上H+的位点,从而抑制SCR反应的吸附、活化和解吸过程,破坏催化循环。为了抵抗碱金属的毒害,人们提出了一些解决方案:1)在催化剂中添加助剂,构筑牺牲位以保护活性组分,例如Yan等[12]采用掺入Ce作为助剂提升催化剂的抗K能力;2)通过构筑核壳结构,将活性组分包覆在里层,阻止其与中毒物质接触[9],例如Yan等[3]基于此思路设计了一种新型TiO2改性的酸处理锰基氧化物八面体分子筛(OMS- 5 (H)@TiO2)高抗碱性能的脱硝催化剂;3)通过构筑碱捕获位点来分离催化剂的活性位点和中毒位点,例如Huang等[13]制备了一种锰钡矿结构(HMO)的锰氧化物催化剂,当该催化剂钾中毒时,K+会自发移动到碱金属捕获位点,因此不会侵害活性位点。
本文将负载铈基催化剂的TiO2载体进行了硫酸化改性,该方法能在保留TiO2氧化还原性的优势的同时,极大地提升催化剂的酸性。同时制备了未经硫酸化改性的催化剂与之对比。通过一系列的表征手段研究了硫酸化改性对铈基催化剂的活性和抗碱金属性能的影响。本文工作可以为抗碱金属中毒催化剂的设计提供一些新的思路。
1 实验部分 1.1 实验原料实验所用的纳米TiO2、H2SO4、Ce(NO3)3·6H2O和KNO3均购于国药集团化学试剂有限公司,纯度为分析纯。
1.2 催化剂的制备载体 将纳米TiO2在H2SO4(0.5 mol/L)溶液中浸渍2 h,倒去上清液,放入烘箱中干燥至恒重。在450 ℃下将干燥后的样品煅烧4 h,此时得到的产物即为硫酸化的TiO2载体,将其标记为TiO2-SO42-。为了比较不同的载体对催化剂性能的影响,同时制备了未经硫酸浸渍改性的TiO2载体。
新鲜催化剂 以Ce(NO3)3·6H2O为铈源将其在上一步制备的TiO2-SO42-(或TiO2)载体上浸渍负载10%(质量分数,下同)的CeO2。具体方法为:将载体与Ce(NO3)3·6H2O的混合物溶于水,在50 ℃下进行旋蒸干燥,将干燥的产物在500 ℃下煅烧2 h。将所得催化剂分别标记为CeO2/TiO2-SO42-和CeO2/TiO2。
中毒催化剂 考虑到在碱金属对催化剂的影响中,K比Na对催化剂的毒害作用更为突出[14],将催化剂浸渍负载K2O模拟烟气中催化剂碱金属中毒的状态。文献[8]报道商用的VWTi催化剂在受到1%(质量分数)的K2O作用时就会完全失活,本研究以此为参考,选择1.2%的剂量进行模拟实验。方法是将KNO3作为钾源,在制备的新鲜催化剂表面浸渍负载1.2%的K2O,将所得催化剂分别标记为K/CeO2/TiO2-SO42-和K/CeO2/TiO2。
1.3 催化剂的表征X射线衍射(XRD)测试由日本理学株式会社的D/max-2200-3KW PC型X射线衍射仪以8(°)/min的扫描速率完成。靶材为Cu靶,λ为0.154 18 nm,测试范围为20°~80°。
催化剂的形貌由德国蔡司公司的SIGMA-300型场发射扫描电子显微镜(FESEM)观测得到。
X射线光电子能谱(XPS)通过美国Thermo Fisher公司的ESCALAB250Xi型光电子能谱仪测试获得,以C 1s的电子结合能284.6 eV进行碳矫正,并利用avantage 5.52软件进行分峰拟合。
氮气吸脱附测试在美国micromeritics公司的ASAP 2460型表面积和孔隙率分析仪上进行,并用Barrett-Joyner-Halenda(BJH)法计算样品的比表面积。
氢气程序升温还原(H2-TPR)测试和氨气程序升温脱附(NH3-TPD)均在美国micromeritics公司的Auto Chem HP 2920型全自动化学吸附仪上完成。
吡啶红外光谱(Py-IR)测试在美国Thermo Fisher公司的Nicolet 6700型光谱仪上完成,该光谱仪配备有Harrick科学红外原位反应池以及汞-镉-碲化物的MCT/A探测器。光谱采集范围设置为1 700~1 300 cm-1,并将记录的数据按照式(3)和式(4)对催化剂中的布朗斯特酸和路易斯酸进行归一化计算[15]。
| $ {{C_{\rm{B}}} = 1.88 \times {A_{\rm{B}}} \times {R^2}/W} $ | (3) |
| $ {{C_{\rm{L}}} = 1.42 \times {A_{\rm{L}}} \times {R^2}/W} $ | (4) |
式中,CB和CL分别为布朗斯特和路易斯酸位的质量摩尔浓度(mmol/g),AB和AL分别为布朗斯特和路易斯酸位的谱带的积分吸光度(cm-1),R为催化剂压片圆的半径(cm),W为样品质量(mg)。
1.4 催化剂的性能测试SCR活性测试在VDRT-200SMT型微型多相催化反应器(衢州Vodo公司)上进行。将催化剂粉末用压片机压片,在20~40目(0.850~0.425 mm)的不锈钢筛网上过筛。称取0.3 g过筛的样品,将其用石英棉固定,放入内径为8 mm的石英管中,测量催化剂的高度。测试时,用氮气作为载气向石英管中通入500×10-6(体积分数)NO、500×10-6(体积分数)NH3、5%(体积分数)O2。用美国Thermo Fisher公司的Antaris系列红外气体分析仪记录出口气体(NO、NO2、N2O和NH3)的体积分数。按照式(5)和式(6)计算NOx的转化率和N2的选择性[16]。
| $ {{X_{{\rm{N}}{{\rm{O}}_x}}} = \frac{{\varphi {{\left( {{\rm{N}}{{\rm{O}}_x}} \right)}_{{\rm{in}}}} - \varphi {{\left( {{\rm{N}}{{\rm{O}}_x}} \right)}_{{\rm{out}}}}}}{{\varphi {{\left( {{\rm{N}}{{\rm{O}}_x}} \right)}_{{\rm{in}}}}}} \times 100\% } $ | (5) |
| $ \begin{array}{*{20}{c}} {{S_{{{\rm{N}}_2}}} = [1 - }\\ {\left. {\frac{{2\varphi {{\left( {{{\rm{N}}_2}{\rm{O}}} \right)}_{{\rm{out}}}}}}{{\varphi {{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_{{\rm{in}}}} + \varphi {{\left( {{\rm{N}}{{\rm{O}}_x}} \right)}_{{\rm{in}}}} - \varphi {{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_{{\rm{out }}}} - \varphi {{\left( {{\rm{N}}{{\rm{O}}_x}} \right)}_{{\rm{out }}}}}}} \right] \times 100\% } \end{array} $ | (6) |
式中,XNOx为NOx(NO+NO2)的转化率;SN2为N2的选择性;φ(NOx)in为气体进口处NOx的体积分数;φ(NOx)out为气体出口处NOx的体积分数;φ(N2O)out为气体出口处N2O的体积分数;φ(NH3)in为气体进口处NH3的体积分数;φ(NH3)out为气体出口处NH3的体积分数。
实验条件下的气时空速由式(7)计算得出[16]。
| $ {V_{{\rm{GHS}}}} = \frac{{{q_{\rm{v}}} \times {{10}^3}}}{{{\rm{ \mathsf{ π} }}{r^2}h}} $ | (7) |
式中,VGHS为气时空速(h-1),qv为气体总流速(L/h),r为反应器的内径(cm),h为催化剂在反应器中的填装高度(cm)。
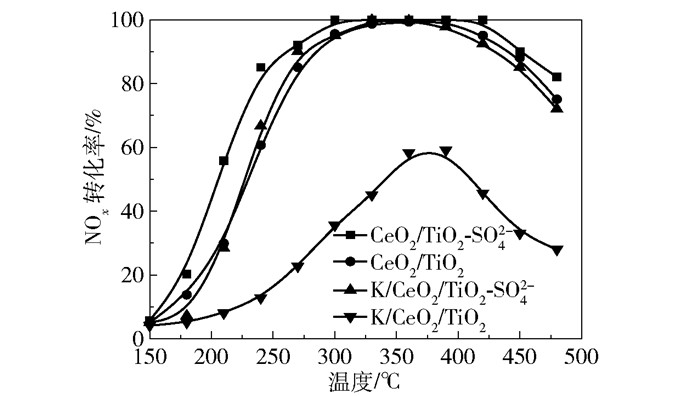
2 实验结果 2.1 催化剂的性能图 1为在气时空速为50 000 h-1的条件下CeO2/TiO2-SO42-、K/CeO2/TiO2-SO42-、CeO2/TiO2和K/CeO2/TiO2 4种催化剂活性测试的结果,发现CeO2/TiO2-SO42-和CeO2/TiO2催化剂的活性远超目前商用催化剂V2O5-WO3的活性(300~400 ℃,NOx转化率为90%)。其中,CeO2/TiO2在290~450 ℃的温度区间内,NOx转化率达到了90%以上。经硫酸化改性后,CeO2/TiO2-SO42-在270 ℃的活性已经达到90%以上,并且在300 ℃时活性达到了近100%,表明硫酸化改性使得催化剂的低温活性明显得到了提升。同时测试了CeO2/TiO2-SO42-和CeO2/TiO2在碱中毒之后的催化活性,发现CeO2/TiO2在受到碱金属作用后催化活性明显下降,NOx转化率最大只有60%,且丧失了温度窗口。而CeO2/TiO2-SO42-在中毒之后,与中毒前相比活性变化小得多,说明硫酸化改性能有效提升催化剂抗碱金属的性能。
|
图 1 不同催化剂的NOx转化率曲线 Fig.1 NOx conversion curves for different catalysts |
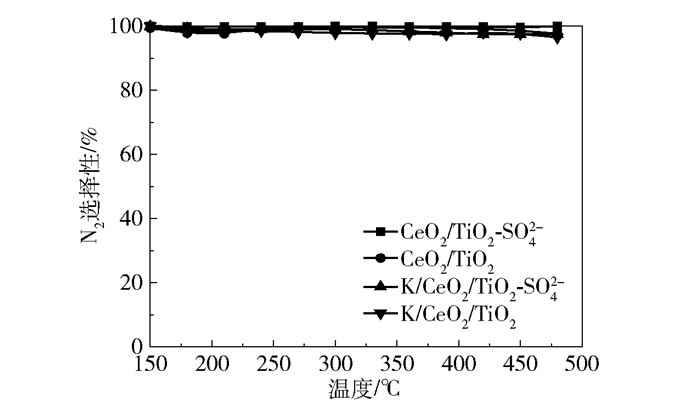
图 2为4种催化剂的N2选择性曲线,发现无论是在硫酸化改性前还是在改性后,催化剂都有着极好的N2选择性。并且在中毒之后催化剂仍有极高的N2选择性,说明碱金属对铈基催化剂的N2选择性影响不大。
|
图 2 不同催化剂的N2选择性曲线 Fig.2 N2 selectivity curves for different catalysts |
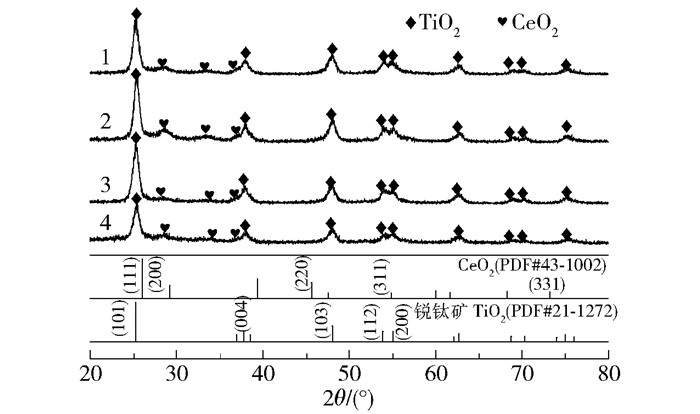
通过XRD测试能够得到催化剂的晶相与结构信息。如图 3所示,在测试的4个样品中均发现归属于锐钛矿TiO2和萤石立方相CeO2的特征衍射峰[17-18]。然而并没有在碱中毒的催化剂中观测到归属于K2O的特征峰,这可能是因为在催化剂中K2O含量太低或是呈无定型分布。另外,通过对催化剂衍射峰强度的对比,发现CeO2/TiO2-SO42-在中毒前后衍射峰强度变化不大,而CeO2/TiO2在中毒之后可以观测到归属于锐钛矿的(101)晶面的衍射峰强度急剧下降。说明碱金属的存在对CeO2/TiO2催化剂产生了某些影响,衍射峰强度降低可能是因为碱金属遮挡了锐钛矿上部分衍射峰的信号。
|
1—CeO2/TiO2-SO42-; 2—K/CeO2/TiO2-SO42-; 3—CeO2/TiO2; 4—K/CeO2/TiO2。 图 3 不同催化剂的XRD图谱 Fig.3 XRD patterns of different catalysts |
利用比表面积和孔隙率分析仪对4种催化剂的比表面积、孔体积和孔径进行了测试,结果如表 1所示。CeO2/TiO2-SO42-和CeO2/TiO2的比表面积相差不大。K/CeO2/TiO2-SO42-的比表面积较CeO2/TiO2-SO42-仅减小了6 m2/g,而K/CeO2/TiO2较CeO2/TiO2的比表面积减小了14 m2/g。这表明碱金属沉积在催化剂表面会使催化剂的比表面积降低,这是由于活性位点被占据且孔道被堵塞所致,同时也是催化剂活性降低的原因之一。而硫酸化改性能够减轻碱金属对催化剂结构的破坏,使催化剂仍能维持较大的比表面积,有利于反应物的吸附和反应[19]。
| 下载CSV 表 1 不同催化剂的比表面积、孔体积和孔径 Table 1 Specific surface areas, pore volumes and pore sizes of different catalysts |
利用FESEM观测了硫酸化改性前后及碱金属中毒前后4种催化剂的形貌,结果如图 4所示。4种催化剂无特殊形貌,均为粒径均一的纳米粒子。

|
图 4 不同催化剂的FESEM图 Fig.4 FESEM images of different catalysts |
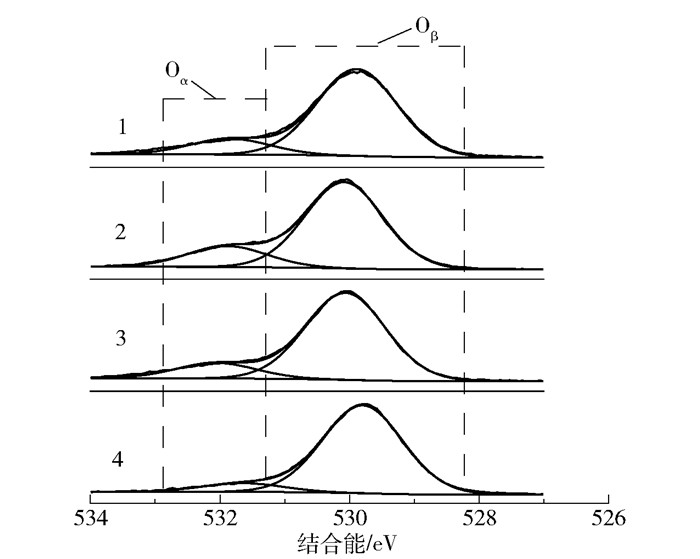
图 5和图 6分别为4种催化剂的O 1s和Ce 3d的XPS光谱。在图 5中,表面吸附氧(Oα)的峰位于531.7 eV附近,晶格氧(Oβ)的峰位于530.4 eV附近。由于Oα在氧化反应中具有较高的迁移率,可以促进NO向NO2转化,促进快速SCR反应的发生,因此在氧化方面比Oβ的活性更高[20]。在图 6中,每条光谱中有8个特征峰,其中,884.8 eV和904.0 eV(分别表示为v和u)处的峰归属于Ce3+,881.6、887.0、898.3、900.8、907.0 eV和916.3 eV(分别表示为v°、v′、v″、u°、u′和u″)处的峰归属于Ce4+[21]。
|
1—CeO2/TiO2-SO42-; 2—K/CeO2/TiO2-SO42-; 3—CeO2/TiO2; 4—K/CeO2/TiO2。 图 5 不同催化剂的O 1s的XPS光谱 Fig.5 O 1s XPS spectra of different catalysts |

|
1—CeO2/TiO2-SO42-; 2—K/CeO2/TiO2-SO42-; 3—CeO2/TiO2; 4—K/CeO2/TiO2。 图 6 不同催化剂的Ce 3d的XPS光谱 Fig.6 Ce 3d XPS spectra of different catalysts |
依据上述的分峰结果,对每个解卷积峰的面积进行了积分,计算了4种催化剂中Ce3+和Oα含量,计算结果如表 2所示。结果表明催化剂的XPS展现出来的规律与其活性结果相一致。由于Ce3+通常伴随着氧空位出现,形成价态未平衡和化学键不饱和的状态,以此提升催化剂表面化学吸附氧物种的数量,促进Ce4+/Ce3+之间的氧化还原循环[22-23]。而K/CeO2/TiO2的Ce3+含量是4种催化剂中最低的,其活性也是四者中最差的。Oα含量的结果也符合这个规律,CeO2/TiO2-SO42-的Oα含量是最高的,碱中毒之后,K/CeO2/TiO2-SO42-中的Oα含量略高于CeO2/TiO2,结果与4种催化剂的活性规律也一致,这也佐证了CeO2/TiO2-SO42-在碱中毒之后活性仍然优异的原因。
| 下载CSV 表 2 不同催化剂的Ce3+和Oα含量 Table 2 Ce3+ and Oα contents of different catalysts |
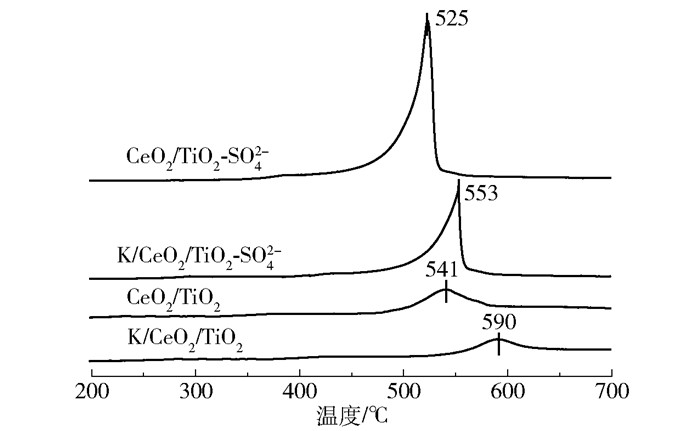
H2-TPR可以评估催化剂的氧化还原能力。如图 7所示,4种催化剂的H2-TPR曲线上均只有1个还原峰。依据该峰的出峰温度可以确定是催化剂中CeO2的表面氧物种被还原[24]。对比CeO2/TiO2-SO42-和CeO2/TiO2的还原峰温度,可以看出载体进行硫酸化处理之后,催化剂的还原峰温度降低了约16 ℃,说明硫酸化改性能够使得催化剂表面的氧物种更容易被还原。另外,对比催化剂的还原峰面积可以发现硫酸化处理极大地增加了催化剂还原的物种的数量。对比CeO2/TiO2-SO42-和CeO2/TiO2在碱金属中毒前后的出峰温度和还原峰面积可以发现,碱金属沉积在催化剂表面会抑制催化剂的氧化还原性能,而硫酸化改性能够有效削弱这一影响。
|
图 7 不同催化剂的H2-TPR曲线 Fig.7 H2-TPR curves of different catalysts |
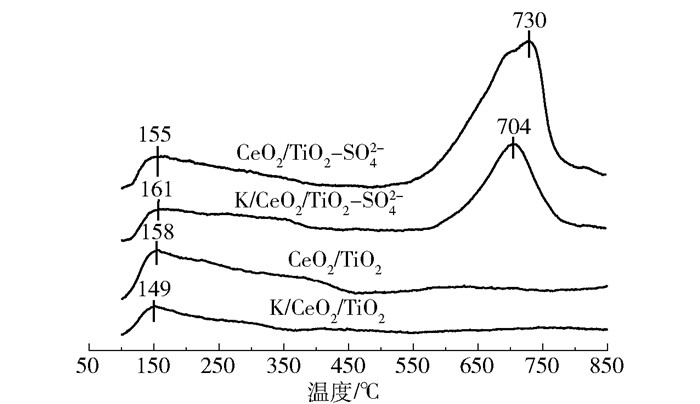
NH3-TPD是表征催化剂酸量的重要手段,可以依据NH3-TPD的出峰温度及峰面积对催化剂的酸量进行判断。图 8为4种催化剂的NH3-TPD曲线,曲线中的峰面积对应于相应样品的酸量[25]。有报道[26]指出,在TPD曲线中,200 ℃以下的特征峰归属于催化剂的弱酸位点,200~400 ℃的峰归属于中强酸位点,400 ℃以上的峰归属于强酸位点,600 ℃以上的特征峰是由硫酸根产生的超强酸位点。硫酸化改性前催化剂中仅有归属于弱酸位点的特征峰,改性后催化剂中不仅有归属于弱酸位点的特征峰,还有归属于超强酸位点的特征峰。对比催化剂改性前后NH3-TPD曲线的峰面积,可以发现硫酸化改性能极大地提升催化剂的酸性。对比催化剂中毒前后的峰面积,可以发现碱金属会损耗催化剂的酸量。CeO2/TiO2的NH3-TPD曲线中仅有归属于弱酸位点的特征峰,该峰的面积在碱金属中毒之后显著减少,酸量显著下降。而CeO2/TiO2-SO42-在碱金属中毒之后,在600 ℃以上其酸量明显减少,而在200 ℃以下酸量并未发生明显变化。由此可以发现在超强酸位点和弱酸位点同时存在时,碱金属会优先损害超强酸位点,从而减少了对弱酸位点的损害,故中毒后CeO2/TiO2-SO42-的活性得以维持。
|
图 8 不同催化剂的NH3-TPD曲线 Fig.8 NH3-TPD curves of different catalysts |
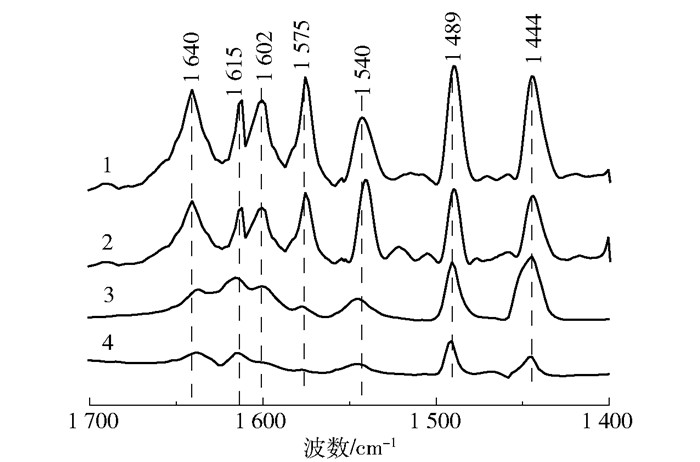
为了确定催化剂表面酸中心的类型,用Py-IR测试了4种催化剂的红外光谱,结果如图 9所示。在1 444 cm-1、1 575 cm-1和1 602 cm-1处出现归属于路易斯酸位点的特征峰,在1 540 cm-1、1 615 cm-1和1 640 cm-1处出现归属于布朗斯特酸位点的特征峰,在1 489 cm-1处出现归属于布朗斯特酸和路易斯酸位点的特征峰[27-28]。
|
1—CeO2/TiO2-SO42-; 2—K/CeO2/TiO2-SO42-; 3—CeO2/TiO2; 4 —K/CeO2/TiO2。 图 9 不同催化剂的Py-IR光谱 Fig.9 Py-IR spectra of different catalysts |
为了定量研究催化剂酸量对催化反应的影响,将4种催化剂的Py-IR测试结果进行了归一化处理,结果如表 3所示。与CeO2/TiO2相比,CeO2/TiO2-SO42-有更多的酸性位点,这是因为硫酸化处理为催化剂带来了大量的酸性中心。对于CeO2/TiO2,未中毒时的酸量远少于CeO2/TiO2-SO42-,而在碱金属中毒之后,酸量基本得不到保留,尤其是路易斯酸性位点。而对于CeO2/TiO2-SO42-,即使在中毒之后酸量也比CeO2/TiO2高,这也与催化剂的活性结果相一致。以上说明CeO2/TiO2在中毒之后,表面的酸性位点会被大量消耗,使得催化剂对NH3的吸附受到影响,阻断了SCR催化循环[29],而CeO2/TiO2-SO42-在中毒之后,催化剂的酸位得以保留,仍能保证对NH3吸附,维持催化反应循环。
| 下载CSV 表 3 不同催化剂归一化的布朗斯特酸和路易斯酸的酸量 Table 3 Amounts of Brønsted acid and Lewis acid sites normalized by different catalysts |
硫酸化改性对铈基催化剂的活性和抗碱金属性能均有提升作用,其原因可以归纳如下:
(1) 硫酸化改性能够减轻碱金属对催化剂结构的破坏,从而维持较大的比表面积,保证反应物的吸附和反应。
(2) 硫酸化改性增加了催化剂表面的化学吸附氧,提高了催化剂的氧化还原性。
(3) 硫酸化处理为催化剂表面提供了大量的酸性位点,在碱中毒之后也能保留足以维持SCR反应循环所需的酸量,从而保障对NH3的吸附。
| [1] |
RICHTER A, BURROWS J P, NÜβ H, et al. Increase in tropospheric nitrogen dioxide over China observed from space[J]. Nature, 2005, 437(7055): 129-132. DOI:10.1038/nature04092 |
| [2] |
GU D, WANG Y H, SMELTZER C, et al. Reduction in NOx emission trends over China: regional and seasonal variations[J]. Environmental Science & Technology, 2013, 47(22): 12912-12919. |
| [3] |
YAN L J, GU Y D, HAN L P, et al. Dual promotional effects of TiO2-decorated acid-treated MnOx octahedral molecular sieve catalysts for alkali-resistant reduction of NOx[J]. ACS Applied Materials & Interfaces, 2019, 11(12): 11507-11517. |
| [4] |
ZHU M H, LAI J K, TUMULURI U, et al. Nature of active sites and surface intermediates during SCR of NO with NH3 by supported V2O5-WO3/TiO2 catalysts[J]. Journal of the American Chemical Society, 2017, 139(44): 15624-15627. DOI:10.1021/jacs.7b09646 |
| [5] |
SMIRNIOTIS P G, PEÑA D A, UPHADE B S. Low-temperature selective catalytic reduction (SCR) of NO with NH3 by using Mn, Cr, and Cu oxides supported on hombikat TiO2[J]. Angewandte Chemie International Edition, 2001, 40(13): 2479-2482. DOI:10.1002/1521-3773(20010702)40:13<2479::AID-ANIE2479>3.0.CO;2-7 |
| [6] |
TANG C J, ZHANG H L, DONG L. Ceria-based catalysts for low-temperature selective catalytic reduction of NO with NH3[J]. Catalysis Science & Technology, 2016, 6(5): 1248-1264. |
| [7] |
ZHANG G D, HAN W L, ZHAO H J, et al. Solvothermal synthesis of well-designed ceria-tin-titanium catalysts with enhanced catalytic performance for wide temperature NH3-SCR reaction[J]. Applied Catalysis B: Environmental, 2018, 226: 117-126. DOI:10.1016/j.apcatb.2017.12.030 |
| [8] |
XU W Q, HE H, YU Y B. Deactivation of a Ce/TiO2 catalyst by SO2 in the selective catalytic reduction of NO by NH3[J]. The Journal of Physical Chemistry C, 2009, 113(11): 4426-4432. DOI:10.1021/jp8088148 |
| [9] |
KAMATA H, TAKAHASHI K, ODENBRAND C U I. The role of K2O in the selective reduction of NO with NH3 over a V2O5(WO3)/TiO2 commercial selective catalytic reduction catalyst[J]. Journal of Molecular Catalysis A: Chemical, 1999, 139(2): 189-198. |
| [10] |
PENG Y, LI J H, SI W Z, et al. Deactivation and regeneration of a commercial SCR catalyst: comparison with alkali metals and arsenic[J]. Applied Catalysis B: Environmental, 2015, 168-169: 195-202. DOI:10.1016/j.apcatb.2014.12.005 |
| [11] |
ZHANG L J, CUI S P, GUO H X, et al. The influence of K+ cation on the MnOx-CeO2/TiO2 catalysts for selective catalytic reduction of NOx with NH3 at low temperature[J]. Journal of Molecular Catalysis A: Chemical, 2014, 390: 14-21. DOI:10.1016/j.molcata.2014.02.021 |
| [12] |
YAN Z D, SHI X Y, YU Y B, et al. Alkali resistance promotion of Ce-doped vanadium-titanic-based NH3-SCR catalysts[J]. Journal of Environmental Sciences, 2018, 73: 155-161. DOI:10.1016/j.jes.2018.01.024 |
| [13] |
HUANG Z W, GU X, WEN W, et al. A "smart" hollandite deNO(x) catalyst: self-protection against alkali poisoning[J]. Angewandte Chemie International Edition, 2013, 52(2): 660-664. DOI:10.1002/anie.201205808 |
| [14] |
PENG Y, LI J H, CHEN L, et al. Alkali metal poisoning of a CeO2-WO3 catalyst used in the selective catalytic reduction of NOx with NH3: an experimental and theoretical study[J]. Environmental Science & Technology, 2012, 46(5): 2864-2869. |
| [15] |
HAO Z F, SHEN Z R, LI Y, et al. The role of alkali metal in α-MnO2 catalyzed ammonia-selective catalysis[J]. Angewandte Chemie International Edition, 2019, 58(19): 6351-6356. DOI:10.1002/anie.201901771 |
| [16] |
YAN L J, JI Y Y, WANG P L, et al. , Alkali and phosphorus resistant zeolite-like catalysts for NOx reduction by NH3[J]. Environmental Science & Technology, 2020, 54(14): 9132-9141. |
| [17] |
HAN L P, GAO M, HASEGAWA J Y, et al. SO2-tolerant selective catalytic reduction of NOx over meso-TiO2@Fe2O3@Al2O3 metal-based monolith catalysts[J]. Environmental Science & Technology, 2019, 53(11): 6462-6473. |
| [18] |
NUGUID R J G, FERRI D, MARBERGER A, et al. Modulated excitation Raman spectroscopy of V2O5/TiO2: mechanistic insights into the selective catalytic reduction of NO with NH3[J]. ACS Catalysis, 2019, 9(8): 6814-6820. DOI:10.1021/acscatal.9b01514 |
| [19] |
王芃芦. 铈钛纳米管负载型核壳催化剂的脱硝活性及其抗中毒性能研究[D]. 杭州: 浙江大学, 2018. WANG P L. The superior NH3-SCR activity and poison resistance of titanate and ceria nanotubes supported deNOx catalysts[D]. Hangzhou: Zhejiang University, 2018. (in Chinese) |
| [20] |
LU J C, WANG J, ZOU Q, et al. Unravelling the nature of the active species as well as the doping effect over Cu/Ce-based catalyst for carbon monoxide preferential oxidation[J]. ACS Catalysis, 2019, 9(3): 2177-2195. DOI:10.1021/acscatal.8b04035 |
| [21] |
WANG S X, GUO R T, PAN W G, et al. The deactivation mechanism of Pb on the Ce/TiO2 catalyst for the selective catalytic reduction of NOx with NH3: TPD and DRIFT studies[J]. Physical Chemistry Chemical Physics, 2017, 19(7): 5333-5342. DOI:10.1039/C6CP07271B |
| [22] |
DUTTA P, PAL S, SEEHRA M S, et al. Concentration of Ce3+ and oxygen vacancies in cerium oxide nanoparticles[J]. Chemistry of Materials, 2006, 18(21): 5144-5146. DOI:10.1021/cm061580n |
| [23] |
CAMPBELL C T, PEDEN C H F. Oxygen vacancies and catalysis on ceria surfaces[J]. Science, 2005, 309(5735): 713-714. DOI:10.1126/science.1113955 |
| [24] |
WANG H Q, CAO S, FANG Z, et al. CeO2 doped anatase TiO2 with exposed (001) high energy facets and its performance in selective catalytic reduction of NO by NH3[J]. Applied Surface Science, 2015, 330: 245-252. DOI:10.1016/j.apsusc.2014.12.163 |
| [25] |
YAN L J, LIU Y Y, ZHA K W, et al. Scale-activity relationship of MnOx-FeOy nanocage catalysts derived from Prussian blue analogues for low-temperature NO reduction: experimental and DFT studies[J]. ACS Applied Materials & Interfaces, 2017, 9(3): 2581-2593. |
| [26] |
ZHAO J, YUE Y H, HUA W M, et al. Catalytic activities and properties of mesoporous sulfated Al2O3-ZrO2[J]. Catalysis Letters, 2007, 116(1-2): 27-34. DOI:10.1007/s10562-007-9085-x |
| [27] |
SUN P F, WANG W L, WENG X L, et al. Alkali potassium induced HCl/CO2 selectivity enhancement and chlorination reaction inhibition for catalytic oxidation of chloroaromatics[J]. Environmental Science & Technology, 2018, 52(11): 6438-6447. |
| [28] |
YAN Q H, CHEN S N, ZHANG C, et al. Synthesis and catalytic performance of Cu1Mn0.5Ox mixed oxide as low-temperature NH3-SCR catalyst with enhanced SO2 resistance[J]. Applied Catalysis B: Environmental, 2018, 238: 236-247. DOI:10.1016/j.apcatb.2018.07.035 |
| [29] |
PENG Y, LI J H, SI W Z, et al. Ceria promotion on the potassium resistance of MnOx/TiO2 SCR catalysts: an experimental and DFT study[J]. Chemical Engineering Journal, 2015, 269: 44-50. DOI:10.1016/j.cej.2015.01.052 |








