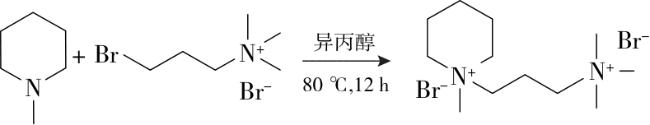
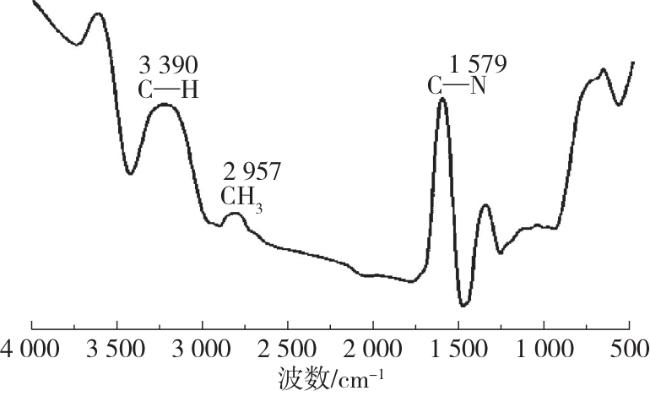
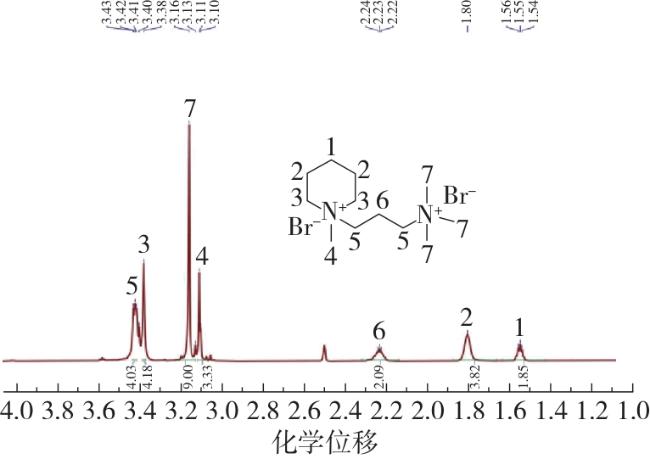
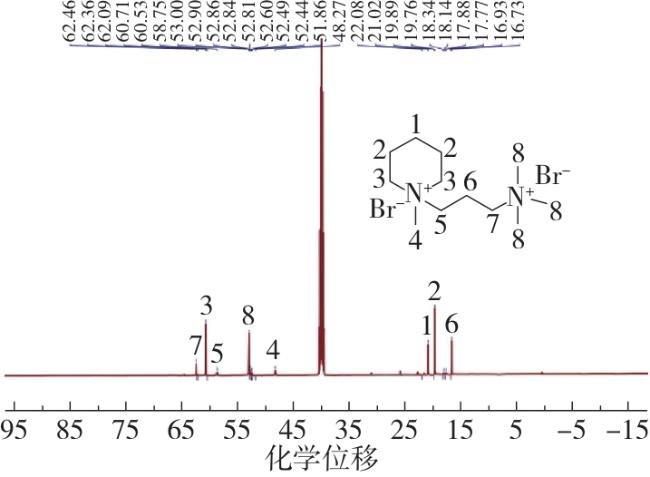
离子液体和低共熔溶剂(deep eutectic solvents,DESs)作为新型绿色溶剂,具有几乎不挥发、几乎不可燃、热稳定性良好和结构可设计性强等特性
[6-11],被认为是分离苯/正己烷混合物的潜在溶剂
[12-18]。目前,已有很多关于离子液体和低共熔溶剂用于萃取分离正己烷中苯的研究。Guo等
[19]比较了环丁砜、1⁃乙基⁃3⁃甲基咪唑双(三氟甲基磺酰)亚胺([EMIM][NTf
2])、1⁃乙基⁃3⁃甲基咪唑硫酸乙酯([EMIM][EtSO
4])和[EMIM][NTf
2]+[EMIM][EtSO
4]混合物对苯/正己烷的分离性能,发现相较于环丁砜,采用离子液体[EMIM][NTf
2]和[EMIM][EtSO
4]作为萃取剂时苯的分配系数和选择性更高,在[EMIM][NTf
2]中加入少量[EMIM][EtSO
4]可显著提高[EMIM][NTf
2]的分离性能。Domańska等
[13]采用离子液体乙基(2⁃羟乙基)二甲基铵双{(三氟甲基)磺酰}亚胺(C
2NTf
2)分离苯/正己烷,在298.15 K下苯的选择性为20。Hansmeier等
[20]采用离子液体3⁃甲基⁃N⁃丁基吡啶双氰胺([3⁃Mebupy][DCA])分离苯/正己烷,在303.15 K下苯的选择性为54.1。Kareem等
[21]采用低共熔溶剂甲基三苯基溴化膦/乙二醇(1∶4、1∶6、1∶8)(除另有说明外,均为物质的量比)分离苯/正己烷,当混合比为1∶6时其分离性能高于环丁砜,当混合比为1∶4时其分离性能高于N⁃甲酰吗啉,此时苯的分配系数和选择性分别为0.346 7和87.085 7。Rodriguez等
[22]以四己基溴化铵/乙二醇(1∶2)和四己基溴化铵/丙三醇(1∶2)作为新型萃取剂用于分离正己烷/苯的混合物,发现在低芳香烃浓度下,当温度为298.2 K时苯在四己基溴化铵/丙三醇(1∶2)中的分配系数大于环丁砜,并且这两种低共熔溶剂对苯的选择性均高于环丁砜。Gonzalez等
[23]比较了不同萃取剂对苯/正己烷的分离效果,发现在常温下氯化胆碱/丙三醇(1∶2)相较于氯化胆碱/乳酸(1∶2)、1⁃乙基⁃3⁃甲基吡啶硫酸乙酯([EMpy][ESO
4])、[3⁃Mebupy][DCA]表现出更高的分离性能,苯的分配系数和选择性分别为0.235 3和53.071 7。虽然以上离子液体和低共熔溶剂相较传统萃取剂对苯/正己烷的分离性能有所提高,但是苯的分配系数和选择性仍较低,不能满足实际分离要求。